その理由は次のとおりです。
* 水分子は極性です: これは、彼らがわずかに正の端(水素原子の近く)とわずかに負の端(酸素原子の近く)を持っていることを意味します。
* 多くの物質も極性です: これらの物質には、正および負の電荷の領域があります。
* likeのように: 極性物質は他の極性物質に引き付けられます。 水分子の正の端は、別の分子の負の端に引き付けられ、逆も同様です。 この魅力は、溶解する物質内の結合を分解し、水と混ぜることができます。
簡単に言えば: 水は小さな磁石のように機能し、他の極性物質の分子を引き離し、広げて溶解することができます。
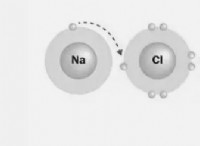
例: 塩(NaCl)は極性物質です。正のナトリウムイオン(Na+)は水分子の負の端に引き付けられ、負の塩化物イオン(CL-)は正の端に引き付けられます。この魅力は塩結晶を分解し、水に溶けます。