酸
* 味: 酸っぱい
* 感触: 腐食性があり、皮膚に燃える感覚を引き起こす可能性があります
* ph: 7未満
* 化学的特性:
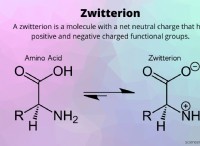
*溶液中に水素イオン(H+)を寄付します。
*塩基と反応して塩と水を形成します。
*青いリトマスペーパーを赤くします。
* 例: 塩酸酸(HCl)、硫酸(H₂SO₄)、クエン酸(柑橘類で見つかった)、酢酸(酢に含まれる)
アルカリ(ベース)
* 味: 苦い
* 感触: タッチに滑りやすい
* ph: 7を超える
* 化学的特性:
*溶液中の水素イオン(H+)を受け入れます。
*酸と反応して塩と水を形成します。
*赤いリトマスペーパーブルーを回します。
* 例: 水酸化ナトリウム(NaOH)、水酸化カリウム(KOH)、アンモニア(NH₃)、水酸化マグネシウム(Mg(OH)₂)
重要な違い
* 水素イオン: 酸は溶液中の水素イオン(H+)を放出しますが、塩基はそれらを受け入れます。
* pHスケール: 酸はpH(0-6)が低く、塩基のpHが高い(8-14)。 7のpHはニュートラルです。
* Litmus Paper: 酸は青いリトマスの紙を赤くし、ベースは赤いリトマス紙を青くします。
* 反応: 酸と塩基は互いに中和し、塩と水を形成するために反応します。
重要な注意: 強酸と強いアルカリの両方は腐食性であり、深刻な火傷を引き起こす可能性があります。注意と適切な安全上の注意を払ってそれらを処理することが不可欠です。