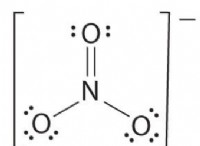
酸を強くするように見えます
* 濃度を増やす: 酸のより濃縮された溶液は、H+イオンの濃度が高くなり、より強く見えるようになります。これは、H+イオンの濃度が高いほど溶液の酸性度が高まり、pH値が低くなるためです。
* 温度を上げる: ほとんどの酸の場合、温度を上げると、イオン化(H+イオンの分離)が増加し、したがって、酸の見かけの強度が増加します。これは、熱が結合を破り、H+イオンの放出を促進するエネルギーを提供するためです。
酸をより弱く見える
* 濃度を減らします: より多くの水を加えることで酸溶液を希釈すると、H+イオンの濃度が低下し、溶液の酸性が低下し、酸が弱くなります。
* ベースを追加: 酸溶液に塩基を追加すると、H+イオンが中和され、溶液が酸性度が低くなり、酸が弱くなります。
重要な考慮事項:
* 強酸と弱酸: 「強い」および「弱い」という用語は、イオン化の範囲を指します 溶液中の酸の。強酸(HClやHNO3など)はほぼ完全にイオン化しますが、弱酸(酢酸など)は部分的にのみイオン化します。 酸の基本強度を変えることはできません。溶液中の見かけの強度のみです。
* 平衡: 酸のイオン化は平衡プロセスです。塩基または希釈を添加すると、酸が非イオン化されていない酸を支持するために平衡がシフトし、弱く見えます。
要約: 酸の強度を根本的に変えることはできませんが、環境を操作して、濃度、温度を調整したり、ベースを追加したりすることで、より強くまたは弱く見えるようにすることができます。