反応:
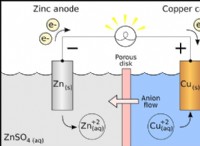
アルミニウム(AL)は、亜鉛(Zn)よりも反応性が高くなっています。これは、アルミニウムが電子を失い、陽性イオンを形成する傾向が強いことを意味します。アルミニウム金属を塩化亜鉛(Zncl₂)の溶液に加えると、アルミニウムは亜鉛を置き、塩化アルミニウム(Alcl₃)と金属亜鉛を形成します。
化学式:
2 al(s) + 3zncl₂(aq)→2alcl₃(aq) + 3 zn(s)
説明:
* 反応物:
*アルミニウム(AL)は固体金属です。
*塩化亜鉛(Zncl₂)は溶存イオン化合物(水溶液)です。
* 製品:
*塩化アルミニウム(Alcl₃)も溶存イオン化合物(水溶液)です。
*亜鉛(Zn)は固体金属です。
観測:
*アルミニウム上の銀色の金属亜鉛コーティングの形成を観察します。
*塩化アルミニウムが溶解すると、溶液が色が変わる可能性があります。
重要なメモ:
*この反応はそれほど活発ではありません。つまり、迅速に発生したり、多くのエネルギー放出が発生したりしません。
*反応は、混合物を加熱することで加速される可能性があります。
*実際の反応は、アルミニウムと水との反応性のため、水が存在する場合、水素ガス(H₂)を生成する場合があります。