主な違い – エタンとエテン
炭化水素は、炭素 (C) と水素 (H) 原子で構成される分子です。炭化水素の大部分は原油に含まれています。エタンとエテンは、分子構造が単純な炭化水素ですが、多くの産業で非常に有用です。エタンは飽和炭化水素です。二重結合はありません。エテンは不飽和炭化水素です。二重結合があります。ただし、どちらも環状構造ではないため、脂肪族炭化水素です。エタンとエテンの主な違いは、エテンの炭素原子は sp 混成であるのに対し、エタンの炭素原子は sp 混成であることです。
対象となる主な分野
1.エタンとは
– 定義、プロパティ、アプリケーション
2.エテンとは
– 定義、プロパティ、アプリケーション
3.エタンとエテンの類似点は何ですか
– 共通機能の概要
4.エタンとエテンの違いは何ですか
– 主な相違点の比較
キーワード:脂肪族、エタン、エテン、エチレン、ハイブリダイゼーション、炭化水素、パイ結合、シグマ結合 
エタンとは
エタンは、2 つの炭素原子と 6 つの水素原子から構成される炭化水素です。構造中に二重結合を持たない飽和炭化水素です。 2つの炭素原子は、共有結合を介して互いに結合しています。水素原子は、単結合を介して炭素原子に結合しています。 3つの水素原子が各炭素に結合しています。エタンの炭素原子はsp混成です。したがって、pi結合を形成するためのハイブリダイズしていないp軌道はありません。したがって、エタンにはシグマ結合しかありません。
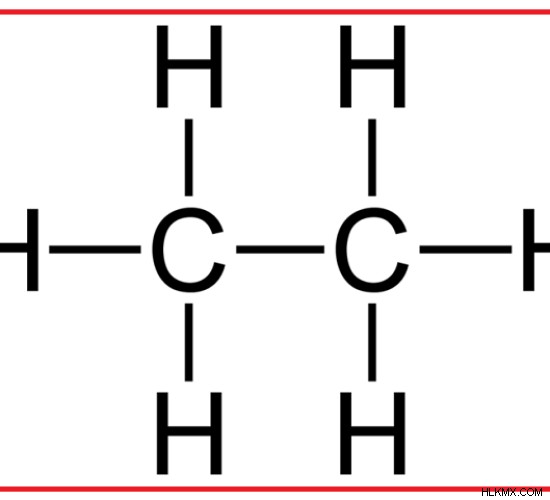
図 1:エタンの分子構造
エタンのモル質量は約 30.07 g/mol です。常温、大気圧で無色無臭の気体です。エタンの融点は約-182.8℃です。エタンの化学式は C2 H6 .二重結合がないため、エタンはアルカンに分類できます。エタンは、天然ガスで 2 番目に重要な成分です。
エタンは可燃性です。したがって、可燃性です。天然ガスの成分です。エタンはまた、エチレンを製造するための反応物としても使用されます。エチレンは多くの産業で不可欠な成分であるため、反応物として非常に重要です。さらに、エタンは、冷却を引き起こす冷凍システムで使用される冷媒です。
エテンとは
エテンは、2 つの炭素原子と 4 つの水素原子で構成される炭化水素です。エテンの化学式はC2 H4 . 2つの炭素原子は、二重結合を介して互いに結合しています。したがって、エテンは不飽和炭化水素です。 2 つの炭素原子は sp ハイブリダイズしています。エテンの分子構造は平面です。
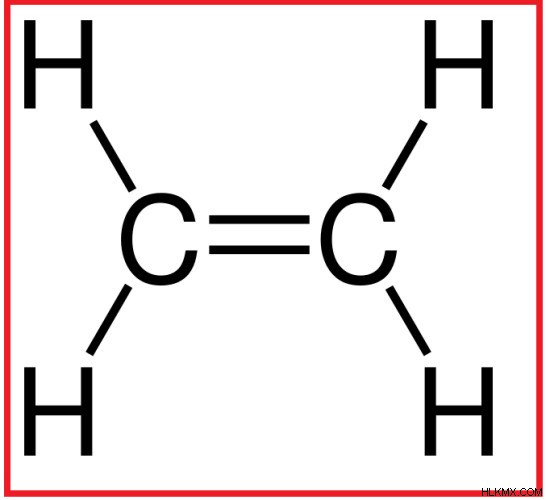
図 2:エテンの分子構造
エテンのモル質量は約 28.05 g/mol です。エテンの融点は-169.2℃です。室温および大気圧では、エテンは特徴的な臭気のある無色の気体です。エテンの結合間の結合角は約 121.3 です。炭素原子はハイブリダイズしていない p 軌道で構成されているため、これらの軌道は 2 つの炭素原子間に pi 結合を形成できます。この二重結合がエテンの反応性を引き起こします。
エテンの通称はエチレンです .エテンモノマーの重合によるポリエチレンなどのポリマー材料の製造に使用されます。エチレンはまた、果実の成熟を調節するホルモンとして、植物において主要な役割を果たします。
エタンとエテンの類似点
- エタンとエテン分子は、炭素原子と水素原子で構成されています。
- どちらも 2 つの炭素原子で構成されています。
- どちらも炭化水素です。
- どちらも脂肪族有機分子です。
エタンとエテンの違い
定義
エタン: エタンは、2 つの炭素原子と 6 つの水素原子で構成される炭化水素です。
エテン : エテンは、2 つの炭素原子と 4 つの水素原子で構成される炭化水素です。
化学式
エタン: エタンの化学式はC2 H6 .
エテン : エテンの化学式はC2 H4 .
炭素の混成
エタン: エタンの炭素原子は sp 混成です。
エテン : エテンの炭素原子は sp 混成です。
モル質量
エタン: エタンのモル質量は約 30.07 g/mol です。
エテン : エテンのモル質量は約 28.05 g/mol です。
融点
エタン: エタンの融点は約-182.8℃です。
エテン : エテンの融点は約-169.2℃です。
結合角度
エタン: エタンの H-C-C 結合の結合角は約 109.6 です。
エテン : エテンの H-C-C 結合の結合角は約 121.7 です。
C-C結合の長さ
エタン: エタンの C-C 結合長は約 154 pm です。
エテン : エテンの C-C 結合長は約 133 pm です。
C-H結合の長さ
エタン: エタンの C-H 結合長は約 110 pm です。
エテン : エテンの C-H 結合長は約 108 pm です。
結論
エタンとエテンの両方が天然ガスの主要成分として見つかります。それらは非常に可燃性で可燃性です。エテンはポリマーを製造するためのモノマーとして使用できますが、エタンはこの目的には使用できません。これは、エタンには二重結合も官能基もないためです。これがエタンとエタンの主な違いです。