その理由は次のとおりです。
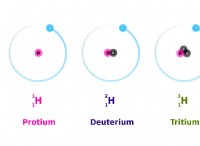
* 極分子 電子密度の不均一な分布を持ち、電荷の分離を作成します。分子の一方の端はわずかに正電荷(Δ+)を持ち、もう一方の端にはわずかに負電荷(Δ-)があります。
* 双極子双極子相互作用 1つの極性分子の正の端が別の極性分子の負の端に引き付けられる場合に発生します。この魅力はイオン結合よりも弱いが、ロンドンの分散勢力よりも強い。
双極子型相互作用による分子の例:
*水(h₂o)
*アンモニア(nh₃)
*塩化水素(HCL)
*一酸化炭素(CO)
重要な注意: 双極子双極子相互作用は極性分子間でのみ発生します。非極性分子(メタン、Ch₄など)には永久双極子モーメントがないため、双極子双極子の相互作用が発生しません。