これがこれが起こる理由の内訳です:
* 原子は作成または破壊されません: 化学反応には、原子の作成や破壊ではなく、原子の再配置が含まれます。 反応物に存在する原子は、単に異なる方法で結合して製品を形成します。
* 化学結合が壊れて形成されます: 反応中に、反応物内の既存の化学結合が破損し、同じ原子の間に新しい結合が形成され、生成物が作成されます。この再配置にはエネルギーの変化が含まれますが、原子の総数は同じままです。
* 質量は原子に関連しています: 原子の数は変化しないため、これらの原子に関連する総質量も一定のままです。
例:
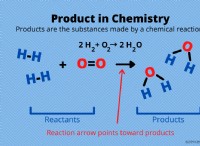
水素ガス(H2)と酸素ガス(O2)の反応を考えて、水(H2O)を形成します。
2 H2 + O2→2 H2O
*反応物:4つの水素原子(2 H2)と2つの酸素原子(O2)
*製品:4つの水素原子と2つの酸素原子(2 H2O)
水素と酸素原子の総数は、方程式の両側で同じです。したがって、反応物の総質量(水素と酸素)は、製品の総質量(水)に等しくなければなりません。
例外:
質量保存の法則はほとんどの化学反応に当てはまりますが、いくつかの例外があります。
* 核反応: これらの反応には、原子の核の変化が含まれます。そこでは、質量をエネルギーに変換できます(アインシュタインの有名な方程式E =MC²で説明されています)。
* オープンシステム: 物質を失うか、獲得できるオープンシステム(たとえば、ガスが逃げる)で反応が起こる場合、質量は厳密に保存されない可能性があります。
要約、 化学反応における質量の保存は、原子がこれらのプロセス中に作成または破壊されないという事実に基づいた基本原則です。原子に関連する質量は、単に異なる構成に並べられます。