その理由は次のとおりです。
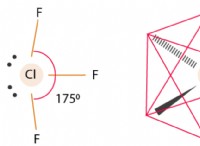
* 構造: アンモニアには、3つの水素原子が付着した中心窒素原子があります。窒素原子には、電子の唯一のペアがあります。
* 水素結合: 水素結合は、水素原子が高強性原子(酸素、窒素、またはフッ素など)に結合し、隣接する電気陰性原子の孤立した電子ペアに引き付けられるときに発生します。
* アンモニアの能力: アンモニアの窒素原子には、容易な電子のペアがあり、これはアクセプターとして水素結合に関与します。 さらに、窒素に付着した水素原子は、水素結合ドナーとして作用する可能性があります。
したがって、単一のアンモニア分子は3つの水素結合に関与できます:
1。ドナーとしての2つの水素結合: 窒素に付着した各水素原子は、別の分子(例えば、別のアンモニア分子または水)に孤立した電子ペアと水素結合を形成できます。
2。アクセプターとしての1つの水素結合: 窒素原子の孤立ペアは、別の分子から水素原子と水素結合を形成できます。
アンモニアは潜在的に3つの水素結合を形成できますが、形成される実際の数は特定の環境と周囲の分子に依存します。