極性は、その温度ではなく、分子の構造の特性です。 その理由は次のとおりです。
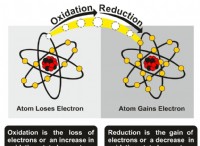
* 電気陰性度: これは、化学結合で電子を自分自身に引き付ける原子の能力の尺度です。 2つの原子間の電気陰性度の違いが大きいほど、結合はより偏光します。
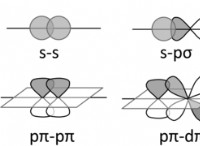
* 分子形状: 分子に極結合が含まれている場合でも、全体的に非極性である可能性があります。これは、分子の対称形状のために極性結合が互いにキャンセルできるためです。たとえば、二酸化炭素(CO₂)には2つの極結合がありますが、その線形形状は非極性分子になります。
極分子の例:
*水(h₂o)
*アンモニア(nh₃)
*塩化水素(HCL)
これらの分子は、すべての温度で極性です 、高温でも。温度は、分子の動きとそれらの相互作用に影響を与える可能性がありますが、固有の極性は変わりません。
要約: 分子の極性は、その構造とその原子の電気陰性度によって決定されます。温度に依存しません。