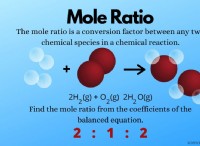
* イオン結合: NaClはイオン結合を介して形成され、1つの原子(ナトリウム、Na)は電子を失い、正に帯電し(Na+)、もう1つの原子(塩素、Cl)が電子を獲得して負の帯電(CL-)になります。
* チャージバランス: 安定した化合物を形成するには、正と負の電荷のバランスをとる必要があります。ナトリウム(Na)には+1電荷があり、塩素(Cl)には-1電荷があります。したがって、1つのナトリウムイオン(Na+)が1つの塩素イオン(Cl-)と結合してNaClを形成し、中性化合物を確保します。
* 電気陰性度: 塩素はナトリウムよりも電気陰性です。つまり、電子に対するより強い魅力があります。これにより、塩素が電子を獲得する可能性が高くなり、ナトリウムはそれを失う可能性が高くなります。
* 価電子: ナトリウムには1つの価電子があり、塩素には7つあります。ナトリウムは、安定したオクテット(外殻に8つの電子)を達成するために1つの価電子を容易に失い、塩素は容易に1つの電子を獲得して安定したオクテットを達成します。
要約: ナトリウムと塩素の化学的特性は、NaClで1:1の比率を形成し、電荷バランスと安定性を確保することを決定します。 NaCl2は、ナトリウムに2つの電子を失う必要があります。これは、電子構成のために非常に好ましくありません。