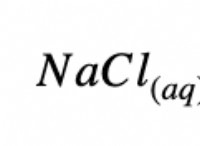材料:
*塩化カリウム(KCl)塩、分析グレード
*蒸留または脱イオン水
*計量紙またはボート
*分析バランス
*ボリュームフラスコ(適切なサイズ、たとえば100 ml、250 ml、500 mlなど)
*攪拌棒
*漏斗
手順:
1。必要なKClの質量を計算します:
* KClのモル質量: 74.55 g/mol
* 望ましい濃度: 0.01 m(モル/リットル)
* 作成したいソリューションの量: ニーズに合わせて便利なボリューム(100 mlなど)を選択してください。
* 式: 質量(g)=モルリティ(mol/l)x volume(l)xモル質量(g/mol)
* 例: 100 mlの解決策:
*質量(g)=0.01 mol/l x 0.1 l x 74.55 g/mol =0.07455 g
2。重量はKCl:です
*分析バランスを使用して、計算されたKCLの質量を慎重に計量します。
*少量の塩を使用して、最初にバランスを満たす必要がある場合があります。
3。 KClを体積フラスコに移し:
*漏斗を使用して計量されたKCLを容積フラスコに静かに転送して、損失を回避します。
*計量紙またはボートを少量の蒸留水ですすぎ、この洗浄をフラスコに移して、すべてのKCLが溶解するようにします。
4。蒸留水を追加:
*体積フラスコを蒸留水で半分ほど満たします。
*フラスコを静かに渦巻かせて、KCLを完全に溶解します。
*溶液がフラスコの首のキャリブレーションマークに達するまで蒸留水を追加し続けます。埋め尽くさないように注意してください。
5。徹底的に混合:
*フラスコがマークに充填されたら、徹底的に停止し、フラスコを数回反転させて、徹底的な混合を確保します。
重要なメモ:
* 純度: 正確な結果を得るには、常に分析グレードKCLを使用してください。
* 体積フラスコ: 体積フラスコは校正されて、特定の量の溶液を正確に供給します。作成するボリュームには、正しいサイズのフラスコを使用します。
* 溶解: フラスコのマークを作成する前に、すべてのKCLが完全に溶解していることを確認してください。
* ストレージ: 蒸発や汚染を防ぐために、標準溶液をしっかりと密閉容器に保管します。
ラベル付け: 次の情報でコンテナに明確にラベルを付けます。
* 解決策の名前: 塩化カリウム(KCL)標準溶液
* 濃度: 0.01 m
* 準備された日付:
* イニシャル:
これらの手順に従うことにより、実験室のニーズに合わせて信頼できる0.01 m KCL標準ソリューションを準備できます。