1。温度: 温度を上げると、分子により多くのエネルギーが得られ、より速く動き、より頻繁に衝突し、より大きな力で衝突します。これにより、衝突がより成功し、反応速度が高くなります。
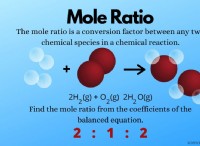
2。濃度: 反応物の濃度が高いということは、反応混合物により多くの反応物分子が存在することを意味します。これにより、反応物分子間の衝突の可能性が高まり、反応速度がより速くなります。
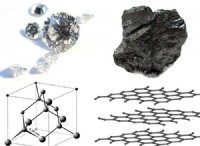
3。表面積: 固体を含む反応の場合、固体反応物の表面積を増やすと、反応が発生するためにより多くの接触点が得られます。木製の火を考えてみてください:酸素にさらされるより大きな表面積があるため、小さなキンドリングは大きな丸太よりも速く燃えます。
4。触媒: 触媒は、その過程で消費されることなく反応を加速する物質です。触媒は、より低い活性化エネルギーを持つ代替反応経路を提供することにより機能します。これは、反応が発生するために必要なエネルギーが少ないことを意味します。