その理由は次のとおりです。
* 電子構成: アルカリ金属には、1つの価電子(最も外側のシェルに電子)しかありません。この単一の電子は簡単に失われ、非常に反応性が高くなります。
* 電気促進性: アルカリ金属は高度に電気依存症であり、陽性イオンを形成するために電子を容易に失います。
* 低イオン化エネルギー: アルカリの金属原子から電子を除去するために必要なエネルギーは非常に低く、反応性にさらに寄与しています。
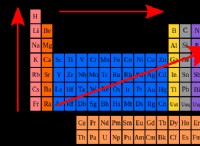
グループ1:を下ると反応性が増加します
* リチウム(li) 最も反応性の低いアルカリ金属です。
* ナトリウム(Na) リチウムよりも反応性が高い。
* カリウム(k) ナトリウムよりも反応性があります。
* ルビジウム(RB) カリウムよりもさらに反応性があります。
* cesium(cs) 最も反応性の高いアルカリ金属です。
* francium(fr) 、非常に反応性もありますが、放射性であるため、めったに遭遇しません。
重要な注意: アルカリ金属は非常に反応性があるため、自然の中で純粋な元素の形では見られません。それらは常に塩のような化合物で見られます。