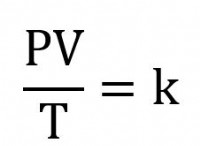ハーバー ボッシュ プロセスは、大気中の窒素と水素を組み合わせて、植物の成長を促進するために使用される肥料の主成分であるアンモニアを生成します。
1909 年から 1910 年にかけて発明されたハーバー・ボッシュ法は、科学分野で行われた最も重要な発明の 1 つです。このプロセスは、ドイツの化学者で発明家であるフリッツ・ハーバーとカール・ボッシュにちなんで名付けられました。このプロセスは、大気中の窒素と水素を組み合わせてアンモニアを生成します。シンプルですね。ええと…違います。
実際、プロセスの発明は非常に重要であり、ハーバーとボッシュはその業績に対してノーベル賞を受賞しました。さて、なぜアンモニアの生産がノーベル賞に値する並外れた偉業と見なされたのか疑問に思われるかもしれません.なぜそれが重要なのかを説明する前に、プロセス自体を見てみましょう。
毎年 4 億トン以上の窒素ベースの肥料が、ハーバー ボッシュ プロセスを使用して生産されています。 (写真提供:NoPainNoGain/Shutterstock)
ハーバー ボッシュ プロセスとは?
ハーバー・ボッシュ法は、大気中の窒素 (N2) を水素 (H2) と結合させてアンモニア (NH3) に変換します。このプロセスでは、単一の窒素分子と 3 つの水素分子が結合して、2 分子のアンモニアが生成されます。ハーバー・ボッシュ過程の化学式は
N2 + 3H2 ⇌ 2NH3
上記の式の ⇌ 矢印は、反応が本質的に可逆的であることを意味します。この反応はたまたま発熱性でもあります。
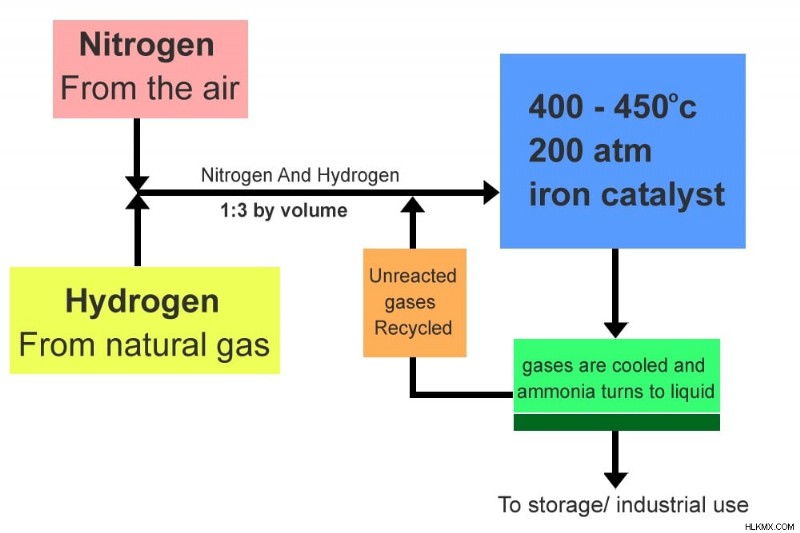
ハーバー・ボッシュ プロセスのフロー図。
水素の主な供給源はメタン (天然ガス) です。実際、世界の総天然ガス生産量の約 3% から 5% がハーバー ボッシュ プロセスで使用され、窒素は大気から直接抽出されます。この反応は、鉄触媒の存在下、および高温高圧下で発生します。
反応装置を通過するたびに、2 つの反応物質の約 15% のみが窒素に変換されます。未反応/未結合ガスは再循環され、再び装置を通過する。生成されたアンモニア分子は、凝縮のために凝縮器を通過し、液体アンモニアが抽出されて貯蔵および工業用に使用されます。
触媒と高圧の役割
大気中の窒素は、二原子分子の形で存在します。分子は、三重共有結合を介して互いに結合しています。これらの結合は非常に強力で、切断するのは困難です。触媒は、窒素分子間のこれらの結合を切断するのに役立ち、またその表面に窒素と水素を吸着します.
元のハーバー・ボッシュ法では、オスミウムを触媒として使用していました。ただし、オスミウムは容易に入手できません。ハーバー ボッシュ プロセスの最新バージョンのほとんどは、代わりに鉄触媒を使用します。 KOH、K2O、Mo、Al2O3 などの促進剤を含む鉄は、反応に完全に多孔質で高表面積の材料を提供します。
化学反応を取り巻く高温と高圧は、化学平衡を回避し、反応が逆方向に進行するのを防ぎます。反応物と生成物の数が時間とともに変化しない場合、反応は化学平衡にあると言われます。
反応初期は窒素と水素の量が多いため、高速でアンモニアが生成されます。 2 つの反応物の濃度が低下すると、変換率が低下します。アンモニアの生成量とアンモニアの分解速度が等しくなる点にすぐに到達します。この状態は化学平衡と呼ばれます。
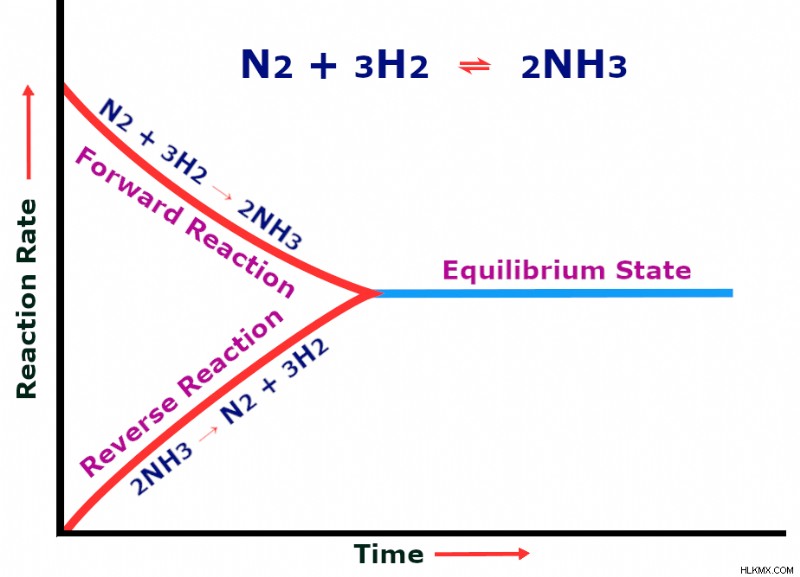
正反応 (N2 + 3H2 → 2NH3) の速度が逆反応 (2NH3 → N2 + 3H2) の速度と等しくなると、平衡状態に達したと言われます。
この時点で、アンモニアはもう生成されていません。アンモニアの生成を継続し、平衡を乱すために、圧力を上げます。 Le Chatelier の原則によると、「システムの圧力を増加させると、生成される分子の数が少なくなり、圧力を下げるのに役立つ反応が優先されます」
ハーバー・ボッシュ法では、窒素と水素の組み合わせにより、生成される分子全体が少なくなります。したがって、反応は順方向に再開し、アンモニアの生成が再開されます。
ハーバー ボッシュ プロセスが重要な理由
ハーバー・ボッシュ法が重要である理由は 2 つあります。第 1 に、このプロセスにより、大気中の大量の窒素を利用できるようになります。第二に、プロセスの最終製品は、世界人口の半分以上を養うのに役立ち続けています.植物が食物を準備する方法と、窒素がそのプロセスに不可欠な理由を見てから説明します.
なぜ植物は窒素を必要とするのですか?
植物は光合成と呼ばれるプロセスを通じて食物を準備します。植物の緑色の原因となる色素であるクロロフィルは、太陽光からエネルギーを吸収し、光合成反応を実行するのに役立ちます.クロロフィル化合物の重要な成分の 1 つは窒素です。したがって、窒素が不足すると、光合成反応が起こらなくなります。窒素は地球上で最も豊富な元素の 1 つですが、窒素欠乏症は植物でよく見られます。
大気中の窒素 N2 間の強力な共有結合により、分子は不活性になり、植物には役に立たなくなります。植物は大気中の窒素を利用できないため、下の土壌で窒素を探します。土壌に存在するバクテリアと古細菌は、N2 分子をアンモニア (NH3) とさまざまな窒素酸化物に変換します。大気中の窒素を分解し、植物にとって有用な形に変換することを窒素固定と呼びます。窒素固定の詳細については、以下をお読みください:窒素循環とは?
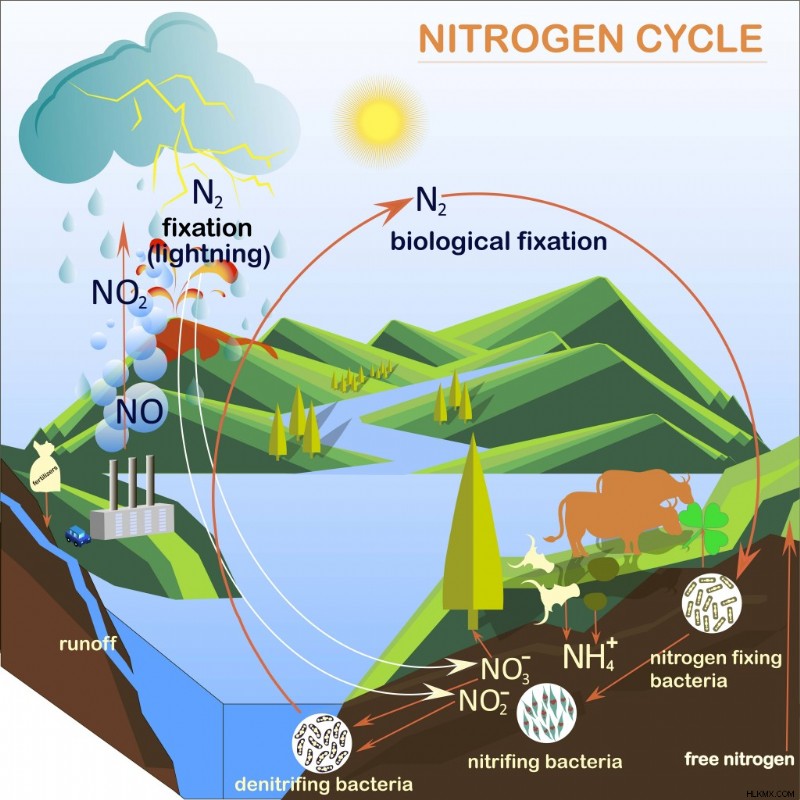
窒素分子の使用可能な窒素 (アンモニアまたは窒素酸化物) への自然な変換は、窒素循環と呼ばれます。 (写真提供:danylyukk1/Shutterstock)
自然に固定される窒素の量は非常に少なく、プロセスは非常に遅くなります。したがって、1900 年代の農家は、輪作などの農業技術を採用するか、牛の糞を肥料として使用して、適切な割合で植物を育てる必要がありました.
ハーバー・ボッシュ法が食料生産に与える影響
ハーバー ボッシュ プロセスの開発により、窒素を人類にとってはるかに有用な形態に、より大量に、より高速に変換することができました。したがって、アンモニアを含む合成肥料は簡単に生産でき、植物の成長を促進するために使用できます。
合成肥料の開発と使用は、前世紀の人口増加を維持する上で重要な役割を果たしてきました。実際、世界の人口は、このプロセスの発見以来 4 倍になりました。 1900 年代初頭の世界人口は約 17 億人でしたが、現在の世界人口はなんと 77 億人に達しています。肥料がなければ、現在生産されている食料の約 3 分の 1 しか利用できません。
結論
肥料が食料生産に与える影響を考えると、ハーバー・ボッシュ法が世界人口の半分以上を養うのに役立ったと言っても過言ではありません。現在、毎年約 4 億から 4 億 5000 万トンの窒素ベースの肥料が、ハーバー ボッシュ プロセスを使用して製造されています。
しかし、肥料はアンモニア由来の製品の 1 つにすぎません。アンモニアのその他の用途には、冷媒としての使用、爆薬の製造、ナイロン/プラスチックの製造などがあります。
なぜハーバーとボッシュがプロセスを発明したことでノーベル賞に値するのか、まだ興味がありますか?世界人口の半分の皿に食べ物を乗せてみてください。あなたも 1 人獲得できるかもしれません!