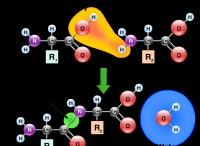
1。重要な違い:プロトンの喪失(H+)
* 酸(HB): 酸は、陽子(H+)を寄付する物質です。 HBの場合、酸には水素原子が付着しています。
* 共役ベース(B-): コンジュゲートベースは、酸がプロトンを失うと形成されます。これは、水素原子が1つ少なく、負電荷があることを意味します。
例:
* 酸(HB): HCL(塩酸酸)
* 共役ベース(B-): cl-(塩化物イオン)
2。重要な特性:
* 酸(HB):
*通常、容易に寄付される水素原子があります。
*中立または積極的に充電される場合があります。
*通常、pHが低い(より酸性)。
* 共役ベース(B-):
*プロトンが失われたため、負の電荷があります。
*必要に応じてプロトンを受け入れることができます(ベースとして機能します)。
*通常、pHが高い(酸性度が低い)。
3。関係:
コンジュゲートベースと酸は、単一のプロトンの獲得または損失によって関連しています。それらは本質的に同じ分子であり、プロトン数に違いがあります。
例:
* 反応: HCl(酸) + H2O(ベース)⇌H3O +(コンジュゲート酸) + Cl-(コンジュゲートベース)
要約:
コンジュゲートベースは、酸がプロトンを寄付した後に残っている種です。酸と塩基の動的な関係を強調するため、酸塩基化学の重要な概念です。