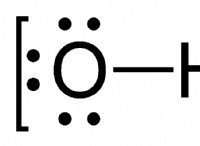その理由は次のとおりです。
* li⁺のサイズが小さく、電荷密度が高い: リチウムイオンは最小で、アルカリ金属イオンの中で最も電荷密度が最も高くなっています。これにより、li⁺と炭酸塩イオンとの間の相互作用が強くなります(Co₃²⁻)。
* 弱いli-O結合: 強力な相互作用により、炭酸塩構造内のLi-O結合が弱くなります。
* 熱安定性: より弱い結合の結果として、炭酸リチウムは比較的低い温度で分解します。加熱時に酸化リチウム(li₂O)と二酸化炭素(CO₂)に容易に分解します。
反応:
li₂co₃(s)→li₂o(s) +co₂(g)
他のアルカリ金属炭酸塩(炭酸ナトリウム、炭酸カリウム、炭酸ルビジウム、および炭酸セシウム)は、陽イオンのサイズが大きくなると相互作用が弱く、M-O結合が強くなるため、より熱安定しています。