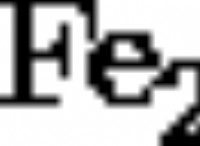反応:
fecl 3 (aq) + zn(s)→zncl 2 (aq) + fe(s)
説明:
* 鉄(iii)塩化物(Fecl 3 ): これは可溶性イオン化合物であり、水に溶けてイオンを形成することを意味します(Fe 3+ およびcl - )。
* 亜鉛(Zn): これは固体金属です。
* 塩化亜鉛(Zncl 2 ): これは、反応の産物として形成される可溶性イオン化合物です。
* 鉄(Fe): これは、反応の産物として形成される固体金属です。
「過剰」部分:
「過剰」という用語は、すべての亜鉛と反応するために必要な鉄(III)が存在することを意味します。これは、反応が完了した後、一部の鉄(III)塩化物が未反応のままであることを意味します。
視覚観察:
*鉄(III)溶液と反応する固体亜鉛金属が観察されます。
*鉄(III)イオンが亜鉛イオンに置き換えると、溶液は黄色から緑がかったものに色を変えます。
*容器の底に濃い灰色または黒い固体(鉄)が形成される可能性があります。
重要な注意: この反応は発熱性であり、熱を放出します。反応混合物は暖かくなったり、熱くなるかもしれません。
要約すると、過剰な鉄(III)と亜鉛の間の反応の生成物は次のとおりです。
* 塩化亜鉛(Zncl 2 )ソリューション
* 固体鉄(Fe)
* 過剰な未反応の鉄(III)塩化物(FECL 3 )ソリューション