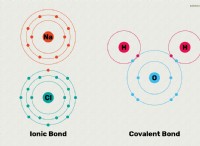
* 炭素(c) 通常、4つの結合を形成します。
* 水素(H) 通常、1つの絆を形成します。
CH2では、カーボンには2つの結合しかあり、2つの不満の折りたたみが残ります。これにより、分子は非常に反応性が高く不安定になります。
考えられるシナリオ:
* カルベン: CH2は、カルベンと呼ばれる非常に反応性のある中間体として存在することができます。カルベンは短命で非常に不安定です。
* 大きな分子の一部: CH2は、炭素原子が他の原子に結合してその原子価要件を満たす大きな分子の一部である可能性があります。たとえば、それはアルケン(エテン、C2H4など)またはより大きな有機化合物の一部である可能性があります。
モル質量:
CH2のモル質量を安定した分子であるかのように計算する場合、炭素と水素の原子質量を追加します。
*炭素(c):12.01 g/mol
*水素(H):1.01 g/mol
Ch2 =12.01 g/mol +(1.01 g/mol x 2)= 14.03 g/mol のモル質量
重要な注意: CH2は単独で安定した分子ではないことを忘れないでください。モル質量計算は理論的なものであり、その式の現実世界の物質には適用されません。