これが簡略化された説明です:
* 酸: 水素イオン(H+)を寄付する物質。
* ベース: 水素イオン(H+)を受け入れる物質。
* 中和: 酸と塩基のプロセスは、反応して中性溶液を形成します。
反応:
酸 +ベース→塩 +水
例:
*塩酸(HCl) +水酸化ナトリウム(NAOH)→塩化ナトリウム(NaCl) +水(H2O)
キーポイント:
*結果の溶液のpHはニュートラルに近い(pH 7)。
*形成された塩は、通常水に溶解する化合物です。
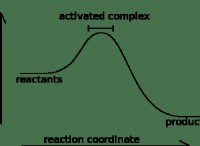
*反応はしばしば熱を放出し、それを発熱性にします 反応。
注: 形成される特定の塩は、使用される特定の酸とベースに依存します。