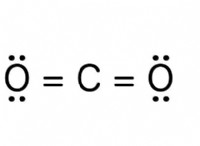極性対非極性分子:単純な故障
極性分子と非極性分子の違いは、電子がどのように分布するかに沸騰します 分子内。
極分子:
* 電子の不均一な分布: 電子は、分子の1つの原子の周りで他の原子よりも多くの時間を費やし、部分的な負電荷を作成します その原子とa 部分的な正電荷 もう一方。これにより、双極子モーメントが作成されます 、分子には小さな磁石のような2つの極があります。
* それを考えてください: 1つのチームがより激しく引っ張り、不均衡を生み出す綱引き。
* 例: 水(H₂O) - 酸素は水素よりも電気陰性であり、電子をそれに近づけます。
非極性分子:
* 電子の偶数分布: 電子は原子間で等しく共有されているため、全体的な電荷はありません 分子で。
* それを考えてください: 両方のチームが等しい強さを持ち、バランスの取れたゲームになります。
* 例: メタン(Ch₄) - 炭素と水素は類似した電気陰性度であるため、電子は均等に共有されます。
重要な違い:
|機能|極分子|非極性分子|
| ----------------- | --------------------------------- | -------------------------------------- |
|電子分布|不均一| |
|チャージ|部分電荷(双極子モーメント)|全体的な料金はありません|
|相互作用|強い分子間力|弱い分子間力|
|溶解度|極性溶媒に溶解します|非極性溶媒に溶解します|
|例|水、アンモニア、エタノール|メタン、二酸化炭素、油|
重要な注意: 分子の形状は、極性を決定する上で重要な役割を果たします。分子に極性結合がある場合でも、形状が対称である場合、極性はキャンセルでき、分子は非極性になります。
極性分子と非極性分子の違いを理解することは、溶解度、融点、沸点などの物理的および化学的特性を理解するために重要です。また、他の分子との相互作用や、さまざまな化学反応における役割を説明するのにも役立ちます。