多くの一般的な塩基、特に水に溶けたものには水酸化物イオンが含まれていますが、機能する他の種類の塩基があります。
1。 Arrheniusベース: これらは従来の塩基の定義であり、水酸化物イオンを含むものです。水に溶解すると、オハイオンが放出され、溶液のpHが増加します。例には、NaOH(水酸化ナトリウム)およびKOH(水酸化カリウム)が含まれます。
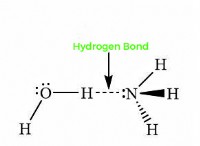
2。 Brønsted-Lowry Bases: このより広い定義は、陽子(H+イオン)を受け入れる物質の能力に焦点を当てています。 これらの塩基には、必ずしも水酸化物イオンを含める必要はありません。例には、アンモニア(NH3)および炭酸イオン(CO32-)が含まれます。
3。ルイスベース: これは、ベースの最も一般的な定義です。ベースを電子ペアのドナーとして定義します。ルイスベースには、必ずしも水酸化物イオンが含まれているわけではないか、プロトン移動に関与する必要さえありません。例には、エーテル、アミン、さらには金属イオンが含まれます。
要約:
* arrheniusベース * do*水酸化物イオンが含まれています。
* brønsted-lowryベース *水酸化物イオンが含まれている場合とそうでない場合があります。
* ルイスベース **必ずしも水酸化物イオンが含まれていません。
したがって、水酸化物イオンが含まれているかどうかを判断するために使用されているベースの特定の定義を考慮することが重要です。