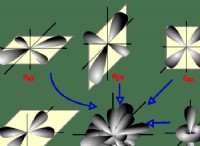
その理由は次のとおりです。
* オゾン構造: オゾンは、他の2つの酸素原子に接続された中心酸素原子を備えた曲がった構造を持っています。
* ハイブリダイゼーション: オゾンの中心酸素原子には、3つの電子ドメイン(2つの単一結合と1つの孤立ペア)があります。これは、SP2ハイブリダイゼーションに対応します。
* ただし: 中央の酸素原子には二重結合もあります。つまり、PI結合のためにそのp軌道の1つを利用する必要があります。これにより、SIGMA結合のために2つのSP2ハイブリダイズ軌道のみが残ります。
したがって、オゾンの中心酸素原子にはSP2ハイブリダイゼーションがありますが、結合の原因となる主要なハイブリダイゼーション状態ではありません。オゾンの中心酸素原子は、Pi結合に使用される1つのp軌道で SP2ハイブリダイゼーションを有すると最もよく説明されています 。