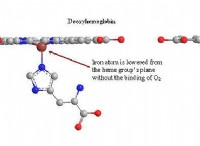
na₂s₂o₃ +4h₂o₂→2naoh +2h₂so₄ +o₂
説明:
* 反応物:
*na₂s₂o₃(チオ硫酸ナトリウム)
*h₂o₂(過酸化水素)
* 製品:
* NaOH(水酸化ナトリウム)
*H₂SO₄(硫酸)
*o₂(酸素ガス)
方程式のバランス:
1。硫黄原子から始めます: 方程式の両側に2つの硫黄原子があります。
2。ナトリウム原子のバランス: 反応物側には2つのナトリウム原子と、生成物側に2つのナトリウム原子があります。
3。酸素原子のバランス: 反応物側には6つの酸素原子、生成物側に8つの酸素原子があります。これのバランスをとるには、h₂o₂の前に4の係数とh₂so₄の前に2の係数を配置する必要があります。
4。水素原子のバランス: 製品側には8つの水素原子、反応物側に8つの水素原子があります。
重要な注意: この反応は酸化還元反応です。チオ硫酸ナトリウムは硫酸に酸化され、過酸化水素は水と酸素ガスに還元されます。
注: この反応は、通常、硫酸が塩基の添加により中和される酸性環境で行われます。全体的な反応は、次のように表現できます。
na₂s₂o₃ +4h₂o₂ + 2naoh→4h₂o +2na₂so₄ +o₂