その理由は次のとおりです。
* 水は極性分子です: 水分子の酸素原子はわずかに陰性であり、水素原子はわずかに陽性です。これにより、双極子モーメントが作成され、水が極分子になります。
* likeのように: 糖、塩、アルコール、酸などの極性物質も、部分電荷を持つ分子で構成されています。 これらの分子の正の端は、水分子の負の端に引き付けられ、その逆も同様です。 水素結合と呼ばれるこれらのアトラクション 、極性分子を水分子に囲まれ、溶解するようにします。
各タイプの物質を分解しましょう:
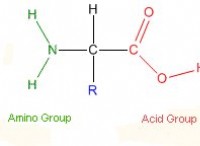
* 砂糖: これらは、水と水素結合を形成できるヒドロキシル基(-OH)を持つ極性分子で構成されています。
* 塩: 塩はイオン化合物です。つまり、積極的に帯電したイオン(陽イオン)と負に帯電したイオン(アニオン)で作られています。陽イオンは水分子の負の端に引き付けられ、陰性イオンは正の端に引き付けられ、塩が溶解します。
* アルコール: アルコールには、糖と同様に水と水素結合を形成できるヒドロキシル基(-OH)があります。
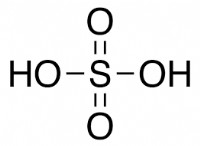
* 酸: 酸は溶液中の水素イオン(H+)を放出します。これらのイオンは、水分子と水素結合を形成し、溶解度に寄与します。
対照的に、油のような非極性物質は、水分子と強いアトラクションを形成するために必要な部分的な電荷が不足しているため、水によく溶けません。