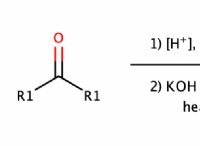
* 塩化ナトリウム(NaCl) :テーブル塩は温水と冷水の両方にかなり溶けますが、お湯に溶けやすいです。
* 硝酸カリウム(KNO3) :この塩は、水温が上昇するにつれて溶解度が大幅に増加することを示します。
* 塩化カルシウム(CACL2) :一般的に脱氷に使用される塩化カルシウムの溶解度は、温度とともに著しく増加します。
* 重炭酸ナトリウム(NAHCO3) :重曹としても知られているこの溶解度は、お湯で著しく増加します。
なぜ一部の塩がお湯に溶けやすいのですか?
塩の溶解度は、次のようないくつかの要因の影響を受けます。
* 温度: 温度が上昇すると、水中の分子はより迅速に移動し、運動エネルギーが増加します。これにより、塩結晶を一緒に保持しているイオン結合を水分子分子が壊れやすくなります。
* 極性: 水は極性溶媒です。つまり、正と負の端があります。これにより、塩結晶中のイオンと相互作用し、それらを引き離して溶解することができます。
* エントロピー: 塩が水に溶けたときに発生するエントロピー(障害)の増加は、溶解度の原動力でもあります。
特定の塩の詳細をご希望の場合はお知らせください!