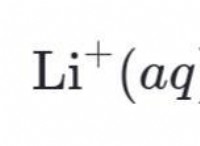塩(NaCl):
* イオン結合: 塩はナトリウム(Na+)と塩化物(Cl-)イオンで構成されています。イオン結合によって結合されています。これらの結合は、特に水のような極性分子が存在する場合、比較的弱いです。
* 極水分子: 水分子は極性です。つまり、わずかに正の末端(水素原子)とわずかに負の末端(酸素原子)があります。
* 溶解プロセス: 塩を水に加えると、極水分子がイオンを囲み、それらを引き離し、イオン結合を破壊します。水分子の正の端は負の塩化物イオンを引き付け、負の端は正のナトリウムイオンを引き付けます。このプロセスは、塩イオンが水全体に分散される溶液を作成します。
sand(sio2):
* 共有結合: 砂は主に二酸化シリコン(SIO2)で作られており、シリコンと酸素原子は強力な共有結合によって一緒に保持されます。 これらの絆は破るのが非常に困難です。
* 非極性構造: 二酸化シリコンは非極性分子であり、水のような陽性と負の端を持っていないことを意味します。
* 不溶性: 強い共有結合と砂の非極性性の性質のため、水分子は砂粒子を効果的に囲み、分離することはできません。したがって、砂はほとんど水中に溶けていないままです。
要約:
*塩は、そのイオン結合と極水分子がそれらの結合を破壊する能力のために水に溶けます。
*砂は強力な共有結合によって一緒に保持され、非極性であり、水分子との効果的な相互作用を防ぐため、水に溶けません。