これが故障です:
* 弱酸/塩基: これらの物質は、溶液中に部分的にのみ解離します。つまり、イオンに完全に分解されません。これにより、酸または塩基を追加して反応し、劇的なpHシフトを防ぎます。
* コンジュゲートペア: 弱酸とそのコンジュゲートベース(または弱い塩基とその共役酸)は、追加の酸または塩基を中和するために連携します。
それがどのように機能するか:
1。酸の追加: 緩衝液のコンジュゲートベースは、添加酸と反応し、それを中和し、pHの大幅な低下を防ぎます。
2。ベースの追加: 緩衝液の弱酸は、追加された塩基と反応し、それを中和し、pHの大幅な上昇を防ぎます。
バッファーの重要性:
バッファーは、以下を含む多くの生物学的および化学システムで重要です。
* 生物学的システム: 緩衝液は、適切な酵素機能と全体的な健康に不可欠な血液、細胞、およびその他の体液のpHを維持します。
* 化学反応: 緩衝液は化学反応で使用され、pHを安定させ、反応が進行するための最適な条件を確保します。
* 産業プロセス: 緩衝液は、食料生産、医薬品製造、廃水処理など、多くの産業プロセスで使用されます。
バッファーの例:
* 血: 重炭酸塩緩衝システム(炭酸/重炭酸塩)は、血液のpHを7.4前後に維持するのに役立ちます。
* リン酸緩衝液: 細胞内液のpHを維持するために重要です。
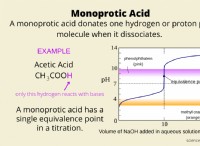
* 酢酸/酢酸緩衝液: 多くの実験室の用途と実験で使用されます。
本質的に、バッファーはpHの衝撃吸収体のように機能し、酸や塩基が導入された場合でも比較的安定した環境を確保します。