その理由は次のとおりです。
* 水素(H) 通常、債券を形成するときに+1充電を運びます。
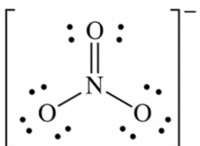
* 多原子イオン イオン内の電子の分布により、正味電荷があります。
例:
* 炭酸イオン(Co3^2-) -2の電荷があります。
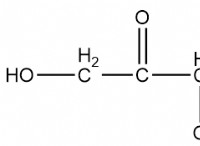
* 重炭酸塩イオン(HCO3-) -1の電荷があります。
炭酸塩(CO3^2-)に水素イオン(H+)を添加すると、重炭酸塩(HCO3-)が形成され、全体の電荷が1つ減少します。
注: この規則には、特に他の要因が電荷に影響を与える可能性のある複雑な多原子イオンでは例外があります。