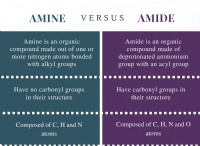
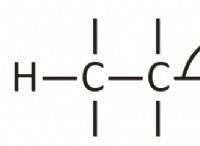1。要素:
* 定義: 通常の化学的手段によってより単純な物質に分解できない純粋な物質。
* 例: 金(au)、酸素(o)、炭素(c)
* 役割: 要素は、すべての問題の基本的な成分です。それらは、他のすべてが構築される基盤です。
2。原子:
* 定義: その要素の化学的性質を保持する要素の最小単位。
* 例: 単一の金原子(Au)、酸素原子(O)、炭素原子(C)
* 役割: 原子は要素の基本的な構成要素です。それらは、電子の雲に囲まれた核(陽子と中性子を含む)で構成されています。
3。イオン:
* 定義: 電子を獲得または失った原子で、正味の正または負の電荷をもたらします。
* 例: ナトリウムイオン(Na+)(電子を失った)、塩化物イオン(Cl-)(電子を獲得)
* 役割: イオンは、イオン化合物を形成するために重要です。それらは静電力(反対の電荷間の引力)を介して相互作用し、強い結合を作成します。
4。分子:
* 定義: 化学的に結合した2つ以上の原子(電子の共有)。
* 例: 水分子(H₂O)、二酸化炭素分子(CO₂)、メタン分子(CH₄)
* 役割: 分子は多くの物質の基礎を形成します。分子内の原子の配置は、その形状、特性、および反応性を決定します。
5。化合物:
* 定義: 固定比で化学的に組み合わされた2つ以上の異なる元素で構成される物質。
* 例: 水(h₂o)、テーブルソルト(NaCl)、砂糖(c₁₂h₂₂o₁₁)
* 役割: 化合物は、私たちが遭遇する多様な一連の材料を作成します。それらの特性は、多くの場合、それらに含まれる要素と劇的に異なります。
全体像:構築物質
* 要素から化合物へ: 元素は組み合わせて、化学的結合を通じて分子と化合物を形成します。
* 構造と特性: 分子および化合物内の原子の配置と結合は、その構造、物理的特性(融点、密度など)、および化学的特性(他の物質との反応)を定義します。
* 物質状態: 分子と分子の動きの間の引力の力は、物質の状態(固体、液体、ガス)を決定します。
要約すると、関係は階層的です:
1。要素 基本的な構成要素です。
2。原子 要素を構成し、要素の最小単位です。
3。イオン イオン化合物を形成する帯電原子です。
4。分子 結合された原子によって形成され、同じ元素の原子(O₂など)を含めることができます。
5。化合物 異なる元素の原子を化学的に結合することによって形成されます。
一緒に、これらのビルディングブロックは、私たちの周りの世界で見られる物質の信じられないほどの多様性と複雑さを生み出します。