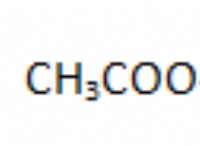* 塩の構造: 塩は、正に帯電したナトリウムイオン(Na+)と負に帯電した塩化物イオン(CL-)で構成されています。これらのイオンは、結晶構造内の強い静電力によって結合されます。
* 水の極性: 水分子(H2O)は極性です。つまり、わずかに正の末端(水素原子の近く)とわずかに負の端(酸素原子の近く)があります。
* 溶解: 塩を水に加えると、極水分子はナトリウムと塩化物イオンを囲みます。水分子の正の端は塩化物イオンを引き付け、負の端はナトリウムイオンを引き付けます。この魅力は、塩結晶を一緒に保持する静電力を克服し、イオンを水全体に分離して分散させます。
結果は、ナトリウムイオンと塩化物イオンが水分子に囲まれ、効果的にそれらを分離するイオン溶液です。 この溶液は、遊離イオンを含むため、依然としてイオン化合物と見なされます。