これが故障です:
* 炭素の結合能力: 炭素には4つの価電子があり、4つの結合を形成することができます。
* 飽和炭化水素: 飽和炭化水素では、各炭素原子は、他の炭素原子または水素原子のいずれかに4つの単一結合を形成します。
* ダブルボンドまたはトリプルボンドなし: 飽和炭化水素は、炭素原子間の二重または三重の結合を欠いています。
例:
* アルカン: 一般式CNH2N+2を備えた最も単純な飽和炭化水素。例には、メタン(CH4)、エタン(C2H6)、およびプロパン(C3H8)が含まれます。
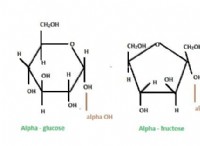
* cycloalkanes: リング構造に配置された炭素原子を備えた飽和炭化水素。例には、シクロプロパン(C3H6)およびシクロヘキサン(C6H12)が含まれます。
なぜ「飽和」という用語?
「飽和」という用語は、炭素原子が水素原子で「飽和」しているという事実を指します。つまり、構造に可能な最大数の水素原子があります。
不飽和炭化水素とのコントラスト:
不飽和炭化水素には、炭素原子間に少なくとも1つの二重または三重結合が含まれています。彼らは、同じ数の炭素原子を持つ飽和した対応物よりも少ない水素原子を持っています。
キーポイント:
* 単一結合のみ: 飽和炭化水素は、炭素原子間に単一の結合しかありません。
* 最大水素: 各炭素原子は、可能な限り最大数の水素原子に結合します。
* アルカンとシクロアルカン: 飽和炭化水素の一般的な例。
* ダブルボンドまたはトリプルボンドなし: これは、それらを不飽和炭化水素と区別します。