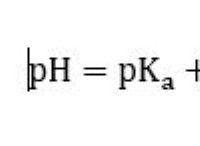これが故障です:
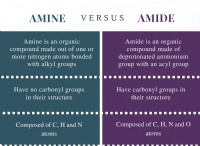
* 機能グループ: これらは、特徴的な化学特性を持つ分子内の原子の特定のグループです。彼らは、分子がどのように他の分子と相互作用するかを決定します。
* 水素結合: 高強性原子(酸素、窒素、またはフッ素など)と別の電気陰性原子の孤立ペアの電子ペアに共有結合した水素原子との強い相互作用。これは、タンパク質やDNAなどの分子の構造と機能にとって重要です。
* イオン相互作用: しばしばカルボキシル基(-COOH)とアミノ基(-NH2)を含む反対に帯電したグループ間の相互作用。これらは、タンパク質の折りたたみおよび酵素活性において重要です。
* 疎水性相互作用: 水を避ける傾向がある非極性グループ間の相互作用。これにより、脂質の凝集とタンパク質の折りたたみが促進されます。
* van der Waals Force: すべての原子間の弱い短距離相互作用。個別に弱いものの、特に大きな分子では、全体的な安定性に大きく寄与する可能性があります。
* サイズと形状: 分子の全体的なサイズと形状も、その相互作用に影響します。これは、3D構造がその機能に不可欠であるタンパク質のような大きな分子に特に当てはまります。
* 化学環境: 分子を取り巻く環境は、その相互作用にも影響を与える可能性があります。たとえば、水や他の溶媒の存在は、分子の溶解度と反応性に影響を与える可能性があります。
要約、 官能基は、大きな有機分子が互いにどのように相互作用するかの重要な決定要因です。これらの相互作用は、生物学的分子の構造、機能、安定性に不可欠です。