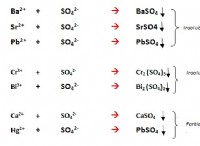
* バリウム(BA) 周期表のグループ2にある金属です。金属は電子を失い、陽性イオン(陽イオン)を形成する傾向があります。
* 窒素(n) 周期表のグループ15にある非金属です。非金属は電子を獲得して負イオン(アニオン)を形成する傾向があります。
バリウムと窒素が反応すると、それらはイオン結合を形成します 。これは、バリウムが2つの電子を失い、ba²⁺陽イオンになることを意味し、窒素は3つの電子を獲得してn³⁻陰イオンになります。 その後、反対に帯電したイオンは互いに互いに互いに引き付けられ、イオン化合物窒化バリウム(ba₃n₂)が形成されます 。
重要な違い:
* 共有結合 2つの非金属間の電子の共有を伴います。
* イオン結合 金属と非金属の間に電子の伝達を伴い、静電引力によって一緒に保持されるイオンの形成をもたらします。