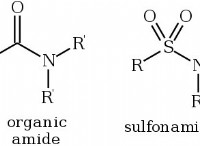
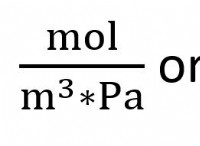これが故障です:
sigma(σ)結合:
* 層: 原子軌道のオーバーラップによって形成されます 内核軸に沿って 、2つの原子の中心をつなぐ想像上の線。このオーバーラップは次の間で発生する可能性があります。
* s軌道 (例えば、H-Hボンド)
* sおよびp軌道 (例えば、h-cl bond)
* p軌道 (たとえば、cl-cl結合、p軌道が真正面から重なります)
* 特性:
* 強い 核間のより大きなオーバーラップと電子密度によるPI結合よりも。
* 単一の結合 2つの原子の間には常にシグマ結合があります。
* 回転 シグマ結合軸の周りで可能です。
pi(π)結合:
* 層: サイドオンオーバーラップによって形成されます p軌道 核核軸に垂直です。
* 特性:
* 弱い 核間のオーバーラップと電子密度が少ないため、Sigma結合よりも。
* シグマ絆に加えて形成 、複数の結合をもたらします (二重またはトリプルボンド)。
* 回転なし これにより、重複が混乱するため、Pi結合軸の周りで可能です。
ここに簡単なアナロジーがあります:
* a sigma bond を想像してください 強いロープとして 2つのオブジェクトを接続し、回転を許可します。
* a pi bond を想像してください 弱い、平らなシート オブジェクトを一緒に保持し、回転を防ぎます。
なぜこれらの用語?
これらの用語は、分子軌道理論に由来します。原子軌道の数学的記述は、その対称性に基づいてSigmaまたはPIとしての分子軌道の分類につながります。
要約:
シグマとPIの結合を理解するのは、の形、強度、および反応性を予測するのに役立ちます 分子の。それらは、さまざまな分子の結合を分析し、それらの物理的および化学的特性を説明するためのフレームワークを提供します。