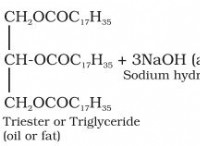* 水は極性分子です: 水中の酸素原子は部分的な負電荷を持ち、水素原子は部分的な正電荷を持っています。この極性により、水分子は他の極性分子を引き付けることができます。
* 水素結合: 水分子は、他の水分子および水素結合能力を持つ他の極性分子との水素結合を形成できます。これらの結合は比較的強力であり、水の物質を溶解する能力に大きく貢献しています。
水に溶ける分子のグループの例:
* 砂糖: グルコースやフルクトースのような糖には、水と水素結合を形成できる多くのヒドロキシル基(-OH)が含まれています。
* アルコール: アルコールには、水と水素結合を形成できるヒドロキシル基(-OH)が含まれています。非極性炭化水素部分がより支配的になるため、炭素鎖の長さが増加するとアルコールの溶解度が低下します。
* カルボン酸: カルボキシル酸には、水と水素結合を形成できるカルボキシル基(-COOH)が含まれています。
* アミン: アミンには、水と水素結合を形成できるアミノ基(-NH2)が含まれています。
* 塩: 塩は、水中のイオンに解離するイオン化合物です。イオンは水分子に囲まれ、水分補給シェルを形成します。
水に溶けない分子のグループの例:
* 非極性炭化水素: 油やグリースのような分子は、主に炭素と水素で構成されており、極性ではなく、水素結合を形成しません。これらの分子は疎水性(水補充)です。
* 脂肪と油: 脂肪と油は、長い非極性炭化水素鎖で構成されており、水に不溶性になっています。
重要な注意: 分子の溶解度は、温度、圧力、他の溶質の存在などの要因の影響を受けます。