その理由は次のとおりです。
* 原子は安定性のために努力します: 原子は、最も外側の電子シェル(価数シェル)が満たされている場合に最も安定しています。
* オクテットルール: ほとんどの原子では、完全な原子価シェルには8つの電子が含まれています(水素とヘリウムを除き、2つだけが必要です)。
* 解決策としての結合: 電子を共有または伝達することにより、原子は安定したオクテット構成を実現できます。これにより、関連する原子のエネルギー状態が低くなり、結合がエネルギー的に好ましいものになります。
ここに、債券の種類の内訳があります:
* イオン結合: ある原子は電子を別の原子に伝達し、互いに引き付ける反対に帯電したイオンを作成します。
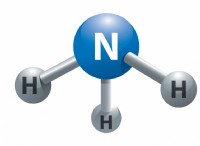
* 共有結合: 原子は電子を共有して、完全な価数シェルを実現します。
* 金属結合: 電子は非局在化され、金属原子の「海」の間で共有されます。
本質的に、化学結合は、安定した電子構成を持つことで原子が可能な限り「幸せ」になりたいために形成され、結合はそれを達成するために使用するメカニズムです。