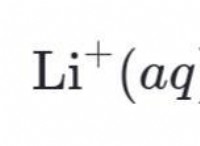その理由は次のとおりです。
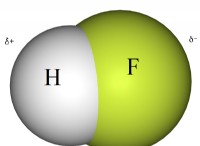
* 極性: 水分子は極性です。つまり、水素側に部分的な正電荷と酸素側に部分的な負電荷があります。イオンは、陽性(陽イオン)または陰性(陰イオン)であろうと、完全な電荷を持っています。
* アトラクション: 反対の電荷が集まり、イオンと水分子の間の静電的相互作用につながります。水分子の正の端は陰イオンに引き付けられ、負の端は陽イオンに引き付けられます。
* 水和シェル: イオンを囲む水分子は水和シェル 。このシェルは、溶液中のイオンを安定化するのに役立ち、他のイオンとの反応を防ぎます。
このように考えてみてください:
正の極と負の極の磁石を想像してください。磁石の近くに正の電荷がある小さな金属ボールを持ってきます。ボールは磁石の負の極に引き付けられます。この魅力は、イオンと水分子間の相互作用に似ています。
キーポイント:
*水和イオンと水の間の結合は、共有結合よりも弱い。
*相互作用の強度は、イオンの電荷密度と水分子のサイズに依存します。
*水和は、多くの化学反応と生物学的プロセスにおいて不可欠なプロセスです。
これ以上質問がある場合はお知らせください!