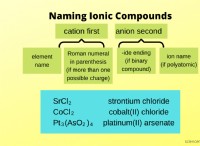
主な違い – 水酸化ナトリウムと水酸化アルミニウム
水酸化ナトリウムと水酸化アルミニウムは金属水酸化物です。水酸化ナトリウムの化学式は NaOH です .水酸化ナトリウムの通称は苛性ソーダです .イオン性化合物です。水酸化アルミニウムは、酸性と塩基性の両方の性質を持つ両性水酸化物です。水酸化アルミニウムの化学式は Al(OH)3 です。 .水酸化ナトリウムと水酸化アルミニウムの主な違いは、水酸化ナトリウムは塩基性化合物であるのに対し、水酸化アルミニウムは両性化合物であることです。
対象となる主な分野
1.水酸化ナトリウムとは
– 定義、化学的性質、用途
2.水酸化アルミニウムとは
– 定義、化学的性質、用途
3.水酸化ナトリウムと水酸化アルミニウムの違いは何ですか
– 主な相違点の比較
重要な用語:水酸化アルミニウム (Al(OH)3 )、両性、ブレンステッド-ローリー塩基、苛性ソーダ、発熱性、吸湿性、ルイス酸、水酸化ナトリウム (NaOH)

水酸化ナトリウムとは
水酸化ナトリウムは、化学式 NaOH を持つ金属水酸化物です。 .水酸化ナトリウムの通称は苛性ソーダです .水酸化ナトリウムは、ナトリウム陽イオン (Na) と水酸化物 (OH) 陰イオンからなるイオン化合物です。強力な基盤です。
水酸化ナトリウムのモル質量は 39.99 g/mol です。水酸化ナトリウムは室温で固体で、不透明な白いろう状の結晶として現れます。無臭です。水酸化ナトリウムの融点は 318 °C、沸点は 1,388 °C です。

図 1:水酸化ナトリウム固体化合物
水酸化ナトリウムは強塩基性化合物であるため、重度のやけどを引き起こす可能性があります。水溶性が高い。水に溶解すると、このイオン化合物はそのイオンに解離します。水へのこの溶解は非常に発熱性です。水酸化ナトリウムは吸湿性です。これは、通常の空気にさらされると、水酸化ナトリウムが空気から水蒸気と二酸化炭素を吸収できることを意味します.
水酸化ナトリウムの用途には、多くの石鹸や洗剤の製造、アスピリンなどの医薬品の製造、水の酸性度の制御、木材を生産する際の不要な物質の溶解などがあります。紙製品など
水酸化アルミニウムとは
水酸化アルミニウムは、化学式 Al(OH)3 を持つ両性水酸化物です。 .両性とは、この化合物が酸性と塩基性の両方の性質を示すことを意味します。水酸化アルミニウムは、ギブサイトとして知られる鉱物として自然界に存在します .
水酸化アルミニウムのモル質量は 78 g/mol です。融点は 300 °C です。水酸化アルミニウムは無定形の白い粉末として現れます。水酸化アルミニウムが酸と反応すると、Brønsted-Lowry 塩基として機能し、プロトンを受け取ります。塩基と反応すると、ヒドロキシル アニオンから電子対を受け取ることにより、ルイス酸として機能します。

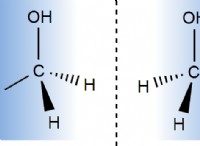
図 2:水酸化アルミニウムの化学構造
水酸化アルミニウムの用途は次のとおりです。
- 他のアルミニウム化合物を生産するための原料
- ポリマー用途の難燃性フィラー
- 人間や動物などの制酸剤
水酸化ナトリウムと水酸化アルミニウムの違い
定義
水酸化ナトリウム: 水酸化ナトリウムは、化学式 NaOH を持つ金属水酸化物です。
水酸化アルミニウム: 水酸化アルミニウムは、化学式 Al(OH)3 を持つ両性水酸化物です。 .
水酸化物陰イオン
水酸化ナトリウム: 水酸化ナトリウムには、ナトリウム陽イオン 1 つにつき水酸化陰イオンが 1 つあります。
水酸化アルミニウム: 水酸化アルミニウムには、1 つのアルミニウム カチオンあたり 3 つの水酸化アニオンがあります。
自然
水酸化ナトリウム: 水酸化ナトリウムは塩基性化合物です。
水酸化アルミニウム: 水酸化アルミニウムは両性化合物です。
モル質量
水酸化ナトリウム: 水酸化ナトリウムのモル質量は 39.99 g/mol です。
水酸化アルミニウム: 水酸化アルミニウムのモル質量は 78 g/mol です。
融点
水酸化ナトリウム: 水酸化ナトリウムの融点は 318 °Cです
水酸化アルミニウム: 水酸化アルミニウムの融点は 300 °C です。
酸との反応
水酸化ナトリウム: 水酸化ナトリウムは酸と反応し、ナトリウム塩を形成します。
水酸化アルミニウム: 水酸化アルミニウムが酸と反応すると、Brønsted-Lowry 塩基として作用し、陽子を受け取ります。
塩基との反応
水酸化ナトリウム: 水酸化ナトリウムは塩基と反応しません。
水酸化アルミニウム: 塩基と反応すると、ヒドロキシル アニオンから電子対を受け取ることにより、ルイス酸として機能します。
結論
水酸化ナトリウムと水酸化アルミニウムはどちらも、金属陽イオンと水酸化陰イオンからなるイオン化合物です。水酸化ナトリウムと水酸化アルミニウムの主な違いは、水酸化ナトリウムが塩基性化合物であるのに対し、水酸化アルミニウムは両性化合物であることです.
参照:
1.「水酸化ナトリウム」。国立バイオテクノロジー情報センター。 PubChem 化合物データベース、米国国立医学図書館、こちらから入手可能。
画像提供:
1. 「水酸化ナトリウムの画像」Hari vinayak santhosh 著 – Commons Wikimedia 経由の自身の作品 (CC BY-SA 4.0)
2. Commons Wikimedia経由のCopsi(パブリックドメイン)による「水酸化アルミニウム」