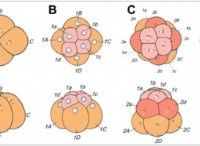
これが故障です:
* 要素 水素(H)、酸素(O)、炭素(C)などの基本的な物質の構成要素です。
* 原子 化学的性質を保持する要素の最小単位です。
原子は互いに結合して、より安定した電子構成を実現します。これはいくつかの方法で発生する可能性があります:
* イオン結合: 1つの原子 *電子は *電子を別の原子に透過し、反対の電荷を持つイオンを形成します。これらの反対の電荷間の魅力は、原子を一緒に保持します。これは金属と非金属の間で発生します。
* 共有結合: 原子 *共有 *電子は、完全な外側のシェルを実現します。これは非金属間で発生します。
* 金属結合: 原子 *プール *電子は、原子を一緒に保持する「電子の海」を作成します。これは金属間で発生します。
すべての要素が他のすべての要素と結合するわけではありません。 ここにいくつかの一般的な傾向があります:
* 金属 非金属と結合する傾向があります 、イオン化合物の形成。
* 非金属 他の非金属と結合できます 、共有化合物の形成。
* 金属 他の金属と結合できます 、金属化合物の形成。
周期テーブル自体は、結合を理解するのに役立ちます:
* グループ1および2(アルカリとアルカリの土の金属) 電子を容易に失い、それぞれ+1と+2のカチオンを形成します。
* グループ17(ハロゲン) 電子を容易に獲得して-1アニオンを形成します。
* グループ18(Nobleガス) 電子の完全な外側の殻を持っていて、一般的に反応しません。
次のことに注意することが重要です:
*これらの一般的な傾向には例外があります。
*形成される結合のタイプは、関連する特定の要素とその電気陰性の違いによって異なります。
*周期表は、結合を理解するための強力なツールですが、各要素の特定の特性を考慮して、それがどのように結合するかを予測する必要があります。