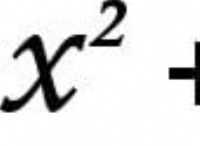* 陽子と中性子: 原子の質量は、主にその核内の陽子と中性子の数によって決定されます。 これらの粒子は、ほぼ同じ質量(約1原子質量単位、またはAMU)を持っています。
* 電子: 電子は陽子や中性子よりもはるかに小さい質量を持っているため、原子のおおよその質量を計算すると無視されることがよくあります。
計算:
* 2中性子 * 1 amu/中性子=2 amu
* 1プロトン * 1 amu/プロトン=1 amu
* 総おおよその質量:2 AMU + 1 AMU =3 AMU
重要な注意: これは単純化された計算です。原子の実際の質量は、結合エネルギーや電子の小さな質量などの要因により、わずかに複雑です。ただし、ほとんどの目的で、陽子と中性子の合計は良い推定値を提供します。