* イオン結合: これは、1つの原子が1つ以上の電子を別の原子に透過すると発生します。これにより、イオン - 正または負の原子が生成されます。反対の電荷が互いに引き付けられ、原子を一緒に保持します。イオン化合物の例には、テーブル塩(NaCl)と塩化カルシウム(CACL2)が含まれます。
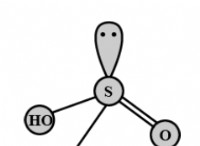
* 共有結合: これは、原子が電子を共有するときに発生します。共有電子は両方の原子の核に引き付けられ、強い結合が生じます。これは、有機分子に見られる最も一般的なタイプの結合です。例には、水(H2O)とメタン(CH4)が含まれます。
* 金属結合: これは、電子が非局在化されている金属で発生します。つまり、特定の原子に結合していないが、金属構造全体を通して自由に移動できることを意味します。これにより、原子間に強い結合が生まれ、良好な導電性や閉鎖性など、金属に特徴的な特性が与えられます。
これらの主要な種類の化学結合に加えて、分子間力もあります 、分子間で発生する弱い力です。これらの力は、沸点や融点など、物質の物理的特性の多くを担当しています。
最終的に、特定の物質の特性を決定するのは、これらすべての力の相互作用です。