何十年もの間、研究者たちは、DNA とその姉妹である RNA が体内を循環していることを発見してきました。これらの分子は、生命のコードを保存し、翻訳するという重要な仕事をしている細胞の安全な内部の外にいます。これらの分子移動の理由は謎のままでしたが、近年、この細胞外 RNA が、少なくとも一部の生物では異なる役割を果たしている可能性があるという証拠が得られています.
遺伝子をタンパク質に翻訳する役割で基礎生物学の学生に最もよく知られている RNA は、驚くほど用途が広く国際的な分子であることが判明しました。植物、回虫、扁形動物、および昆虫は、RNA を使用して、組織全体にシグナルを伝達します。ケンブリッジ大学の分子遺伝学者であるエリック・ミスカは、RNA が生物間、さらには異なる種の間の相互作用において役割を果たしている可能性があることを示唆する実験室での研究に触発されて、「社会的 RNA」という用語を作り出しました。
植物とそれらに感染しようとする害虫は、お互いに対して RNA を配置することができます。 10 月に Science に掲載された論文で、研究者たちは、菌類 (灰色かび病による作物の破壊と、デザート ワインの風味を付ける貴腐菌の生成の両方に関与する菌類) が、自身の小さな RNA 分子を使用して植物の RNA 防御をハイジャックすることによって、どのように自分自身を保護するかについて説明しています。通常は真菌感染症と戦う遺伝子をサイレンシングします。このような発見は、植物と寄生虫の間の軍拡競争における RNA の役割を示しており、これは社会的 RNA の潜在的な例の 1 つです。 「とてもエキサイティングだと思いますが、まだ始まったばかりです」とミスカは言いました。 「まだ多くのことを発見する必要があります。」
植物や無脊椎動物におけるシグナル伝達における RNA の役割は完全には理解されていませんが、その役割は明確に確立されています。これは、ヒトを含む哺乳類の RNA には当てはまりません。これらの種では、科学者はこれらの分子が細胞外を移動していることを知っていますが、それらがコミュニケーションの形態であるかどうかはまだ明らかではありません.
RNA は、血液、尿、涙、脳脊髄液、母乳、羊水、精液など、さまざまな体液から発見されています。さらに、科学者たちは、循環している RNA の小さなビットが、がん性腫瘍や妊娠関連疾患の存在などの特定の状態を反映している可能性があることを発見しました。循環 RNA の発見について、マサチューセッツ総合病院の神経遺伝学者 Xandra Breakefield 氏は次のように述べています。 「私たちは、これらすべてがそこにあることに気づきませんでした。」
細胞外 RNA と DNA が残骸以上のものであることに懐疑的な人もいますが、Brekefield らは、これらが人間の健康に役割を果たす細胞間の通信の新たに発見された形態である可能性があるという、よりエキサイティングな見通しを見ています。たとえば、いくつかの研究では、small RNA が免疫応答の調整やがん細胞の健康な組織への侵入を準備する命令として機能することが示唆されています。
沈黙の合図
1950 年代後半から、RNA (リボ核酸) は、より知名度の高い姉妹 DNA (デオキシリボ核酸) のしもべとしてキャストされました。この役割は、遺伝子コードを転写し、それを細胞を構築して有効にするタンパク質に組み立てることを含むことが判明しました。それらが機能します。しかし、ここ数十年で、RNA の役割は拡大しました。それは、化学反応を開始し、細胞内の遺伝子の活動を調節し、現在では、1 つの細胞が他の細胞の挙動に影響を与えることを可能にする信号として機能することを示唆する人もいます.
約 15 年前、研究者は回虫 Caenorhabditis elegans を作ることができると考えました 筋肉繊維のタンパク質の原因となる遺伝子の配列と一致する RNA の相補鎖を注射することで、けいれんを起こします。この二本鎖 RNA の到着は、標的遺伝子を効果的にオフにするプロセスを開始し、この場合、線虫の筋肉に損傷を与えます。
その後、科学者たちは多くの生物でこのタイプの RNA サイレンシングを発見しました。彼らは、一時的に二本鎖RNAとして存在する可能性のある侵入ウイルスの活動を遮断することにより、感染を防ぐのに役立つと信じています.この二本鎖 RNA が線虫の細胞内に現れると、線虫の分子機構はそれをガイドとして使用して、それを生成したウイルス遺伝子を遮断します。このプロセスは RNA 干渉と呼ばれ、分子チャネルを介してワーム全体に広がる RNA サイレンシング シグナルも生成します。同様のシグナルが、昆虫、扁形動物、植物の体内に広がることが示されています。
植物と無脊椎動物における社会的 RNA の証拠は必然的に疑問を提起します:私たちについてはどうですか?植物や無脊椎動物と同様に、哺乳類は RNA 干渉によって遺伝子をサイレンシングすることができますが、このシステムは私たちの免疫システムで主要な役割を果たしているようには見えません。これまでのところ、哺乳類細胞がワーム細胞のように RNA サイレンシング シグナルをブロードキャストできるという証拠はありません。しかし、microRNA と呼ばれる別の種類の RNA が哺乳類で同様の社会的役割を果たしているのではないかと疑う人もいます.
マイクロRNA経路はRNA干渉経路に関連していますが、マイクロRNAはいくつかの重要な点でRNA干渉に関与する分子とは異なります.マイクロRNAはゲノムにコードされ、同じ生物の他の遺伝子を調節します.感染ウイルスの遺伝子を沈黙させる RNA 干渉とは異なり、マイクロ RNA は、それらが産生される細胞内の遺伝子の発現を低下させます。
マイクロRNAが細胞内で果たす役割はよく理解されていますが、マイクロRNAが細胞外に浮遊している理由は明らかではありません.一部の哺乳類細胞は、小胞と呼ばれる細胞間パッケージを吐き出し、他の細胞に取り込まれます。 2007 年、研究者は哺乳類細胞がマイクロ RNA を含む RNA をこれらのパッケージに挿入できることを発見しました。この発見は、ある細胞が別の細胞の活動に影響を与える新しい方法を示唆しています。
「一部の細胞は、これらの小胞に多くの特定の RNA を入れていることがわかっています」と Breakefield 氏は述べています。 「それらは間違いなく[他の細胞によって]飲み込まれているだけなので、この方法で情報を転送する可能性があります。」
その後、さまざまな RNA やその他の分子、さらには DNA の断片までもが小胞に押し込まれていることが判明し、小胞はマイクロ RNA の唯一の乗り物ではないことが判明しました。この分子は、タンパク質に結合して体内を循環し、細胞外の敵対的な環境から分子を保護します。
証拠と不確実性
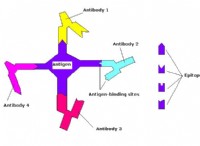
循環マイクロRNAが何をしているのかを理解するために、科学者は、これらの分子が実際にある細胞から別の細胞に移されることを確認する必要があります.細胞は多くのマイクロRNAを産生するため、特定のマイクロRNAがどこで発生したかを特定することは困難です。この問題を解決するために、アムステルダムの VU 大学医療センターの細胞生物学者である D. Michiel Pegtel と同僚は、ウィルス、Epstein-Barr に目を向けました。ウイルスは、感染した細胞に、ウイルスの複製を助けるウイルスマイクロRNAを強制的に生成させます。通常の細胞ではウイルスマイクロRNAを産生しないため、追跡は比較的容易です。
Pegtel と同僚は、2 種類の免疫細胞から始めました。ウイルスに感染した白血球の一種であるB細胞と、ウイルスの侵入者を感知して他の免疫細胞に警告する樹状細胞。この 2 つは、ベシクルのみが通過できるように十分に小さい細孔を備えた膜によって分離されていました。
樹状細胞は、ウイルスが B 細胞に強制的に産生させたマイクロ RNA がバリアを越えて移動し、光っている遺伝子を静めるまで、光るように遺伝子操作されていました。 2010 年に全米科学アカデミー紀要に掲載された結果は、膜を横切る小胞の移動が実際に光る細胞を薄暗くすることを示しています。
しかし、誰もが納得しているわけではありません。この実験や他の RNA 転移実験の結果には、別の説明がある可能性が高いと、ロックフェラー大学の核酸化学者で生化学者である Thomas Tuschl 氏は述べています。小胞と細胞の融合は、ウイルス感染に似ています。したがって、Tuschl は、融合プロセスに関する何か、または多くの異なる種類の分子を運ぶことができる小胞内の何かが、細胞内で免疫反応を引き起こすのではないかと考えています。これにより、到着した RNA の想定される効果に似た細胞の変化が引き起こされる可能性がある、と Tuschl 氏は述べた。
ペグテル氏は、その可能性は低いと述べた。追加のテストでは、ウイルスRNAが樹状細胞に配置された場合、ウイルス自身の遺伝子の1つを標的にすることが示されました.さらに、光っている樹状細胞の減光の程度は、樹状細胞を攻撃したウイルス RNA を含む小胞の量に対応していた、と彼は言いました。ウイルスマイクロRNAを欠く小胞は、減光効果を示さなかった.
それにもかかわらず、Tuschl は他の理由から、哺乳動物の細胞間シグナル伝達におけるマイクロ RNA の役割に懐疑的です。これらの小さな RNA は低濃度で存在し、哺乳動物は植物や無脊椎動物とは異なり、RNA シグナルを増幅する重要なメカニズムを持っていません。 「一般的に、これを効果的なシグナル伝達メカニズムにするには、すべてが少なすぎます」と Tuschl 氏は述べています。
他の人も懐疑的です。スタンフォード医科大学の遺伝学者 Mark Kay は、細胞外マイクロ RNA がこの目的を果たしている可能性を否定していませんが、受け入れる準備はできていません。 「私は心を開いておくように努めていますが、この時点でシグナル伝達が哺乳類のシステムで発生しているとは確信が持てないと思います」とケイは言いました.
ペグテルでさえ慎重であり、循環する RNA が細胞に到達すると特定の変化を引き起こすことを科学者が断言できるようになるまでには、まだ道のりがあると述べています。これまでの哺乳類研究のほとんどは、生きている哺乳類ではなく、試験管内で増殖する細胞で行われてきました。ペグテルが指摘したように、これらの実験は、高濃度のベシクルやマイクロRNAなどの不自然な条件に依存しています。彼は言った、「その効果は非常に人為的です。」
次のステップは、生きている哺乳類の非常に複雑な中で、小胞が運ぶ RNA が意味のある効果を持っていることを示すことである、と彼は言いました。 「時が経てばわかります。」
新しい一連の実験は、質問に答え、人間の健康と病気における循環 RNA の役割を明らかにするのに役立つ可能性があります。国立衛生研究所は 8 月に、マイクロ RNA を含む細胞外 RNA の理解と、これらの分子を使用した疾患の診断と治療に焦点を当てた 24 の研究プロジェクトに 1,700 万ドルの資金を提供したと発表しました。
助成金の 1 つを受け取った Breakefield は、非常に悪性度の高い脳腫瘍である神経膠芽腫から放出された RNA が、周囲の細胞を操作して自身の成長をサポートする方法を調べています。助成金受領者でもある Tuschl は、自己免疫疾患のマーカーとして RNA を使用する可能性を探っています。別の助成金を通じて、彼はまた、RNA を含む小胞の到着に続く細胞の変化の潜在的な別の説明を研究したいと考えています.
NIH の観点からは、この RNA がシグナルとして機能する可能性があるという証拠がすでに示されています。しかし、移動する RNA が破片にすぎないとしても、病気のマーカーとして、また、到達困難な場所に薬を届けるために RNA を運ぶ小胞を徴集する手段として、まだ使用されている可能性があると、 NIH の細胞外 RNA プログラムに関与している国立トランスレーショナル サイエンス推進センター。
細胞生物学と医学への影響は包括的なものである、と Tagle は述べた。 「ある意味で、私たちは新しい研究分野を開拓しています」と彼は言いました。