中学化学科では酸塩基中和反応は非常に重要な教科であり、高校入試化学試験の核心教養でもあります。それでは、酸塩基中和反応の本質を学びましょう。
酸塩基中和の本質
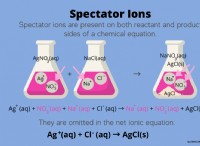
中和反応とは、酸と塩基の成分が交換して塩と水になる反応(酸+塩基→塩+水)のことです。その本質は、H+ (水素イオン) と OH- (水酸化物イオン) が結合して水を形成することです。
酸と塩基は水に溶け、水中で自由に動く陰イオンと陽イオンにイオン化されます。例えば、HCl(塩酸)は水素イオン(H+)と塩化物イオン(Cl-)に電離し、NaOH(苛性ソーダ)はナトリウムイオン(Na+)と水酸化物イオン(OH-)に電離します。水素イオンと水酸化物イオンが結合してイオン化するのが非常に困難な水を形成するため、溶液中に残るのはナトリウムイオンと塩化物イオンです。ナトリウムイオンと塩化物イオンは溶液中でイオン化されたままであり、結合しません。しかし、製品はNaCl(塩)です。したがって、中和反応の本質は、酸と塩基が反応して塩と水を形成することです。
酸塩基中和反応の中和熱
中和熱とは、希薄溶液中で酸とアルカリを中和して1molの水を生成する反応熱のことです。一塩基強酸と強塩基の中和熱は約57kJで、これは酸と塩基の種類に関係なく、実際には1molH+と1molOH-が1molH2Oを生成する反応熱です。弱酸、弱塩基、多塩基酸の中和熱は電離熱の影響で一定値にはなりません。
ポリ酸の中和反応は、通常、熱効果を減少させます。たとえば、H3PO4 は NaOH で中和され、1 モルの塩基を加えることによる中和熱は -64.86kJ、2 番目の 1 モルの塩基を加えることによる中和熱は -56.85kJ、3 番目の 1 モルの塩基を加えることによる中和熱は -56.85kJ です。塩基のモルは -56.85kJ 熱は -2.0gkJ です。
上記は、酸塩基中和反応の一般的なテスト ポイントです。実際の生産用途では、人々はしばしば酸塩基中和を使用して、土壌の酸性度とアルカリ度を改善し、過酸性度を処理し、廃水を処理します.