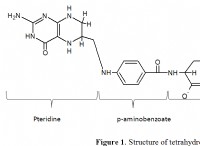
BrF5 または五フッ化臭素は、その高い毒性と腐食性でよく知られている化合物です。この化合物の他の特性には、強い臭気と無色が含まれます。その製造方法には、臭素を150℃以上の温度で大量のフッ素で処理することが含まれます。用途、化合物の電子配置、分子構造、結合角など、別の一連のプロパティもあります。 BrF5 の分子構造は四角錐形で、結合角はそれぞれ 90° です。
BrF5 または五フッ化臭素
BrF5 はハロゲン間化合物です。つまり、この化合物の分子には 2 つ以上の異なるハロゲン原子が含まれていますが、他のグループに属する元素の原子は含まれていません。この化合物の電子配置は、sp³d² として表すことができます。この有毒で腐食性のある化合物の用途については、主にロケットの推進剤やウランの処理に使用されます。
この化合物に存在する価電子は合計 42 個です。ロケット推進剤やウラン処理装置の他に、さまざまな分析や実験目的にも使用されます。
分子幾何学
分子を構成する原子の三次元配列の構造を分子幾何学と定義します。さまざまな化合物が分子構造を持っています。ここでは、1 つの特定の化合物、五フッ化臭素の分子構造に焦点を当てます。色、磁性、化合物の生物学的活性、反応性、物質の相、極性など、化合物の特性の一部に影響を与える可能性があります。 BrF5 の分子構造に関しては、四角錐形です。
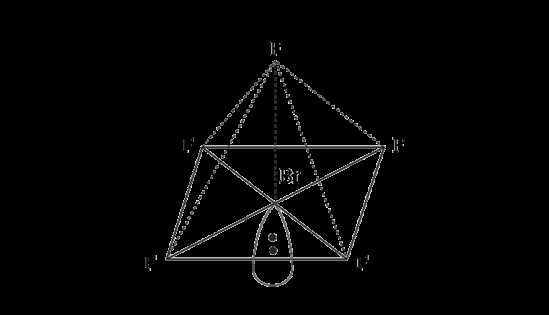
正方錐体分子構造とは
すでに説明したように、BrF5 の分子構造は四角錐です。四角錐の形状は、分子内に 5 つの結合と 1 つの孤立電子対がある場合に形成される分子の形状として定義できます。形状を観察すると、化合物の形状は ML5 式で表されます。ここで、L は配位子、つまり化合物の他の原子を中心原子に結合するイオンまたは原子です。四角錐の分子構造は、アクティブな非共有電子対で構成される主なグループの特定の化合物の一般的な形状です。
結合角
任意の化合物の結合角は、特定の化合物、分子、または複合体の 1 つの中心原子と電子の結合対の軌道の間の角度として定義できます。また、化合物の幾何学的形状と性質を特定するのにも役立ちます。たとえば、二酸化炭素 (CO2) の結合角は 180° です。この情報から、CO2 の幾何学的形状は線形であると結論付けることができます。
H2O の別の例を参照してください。酸素原子には 6 個の電子があり、そのうち 2 個が水素原子と結合し、孤立電子対が 2 つ残ります。したがって、この結合により、H2O の 1 つの分子は、それらの間に 104.5° の結合角を持ちます。
化合物 BrF5 の結合角
BrF5 または五フッ化臭素の結合角は 90° です。したがって、中心原子と他の原子との間で形成される角度は、それらの間で 90° の角度になります。五フッ化臭素の 90° 結合角の総数に関しては、化合物は原子の 5 つの結合対と 1 つの非共有電子対で構成されます。また、90° の完全な結合角は存在しないことにも留意する必要があります。
化合物の結合角の計算方法
結合角の測定値は、それらの間に存在する孤立電子対の数に依存します。化合物の結合角を見つけるための最も一般的な方法は、VSEPR 理論にまで遡ります。 VSEPR 理論は、化合物の形状を調べるために使用されるため、化合物がその中に持つ結合角の測定値を知るのに役立ちます。この理論は、分子内の各原子が、その特定の原子の原子価殻内の電子間の反発力を最小限に抑える幾何学的形状を達成すると述べています。たとえば、アンモニアには 1 つの孤立電子対があり、その幾何学的形状は三角錐です。したがって、結合角は 107.5° です。
結論
BrF5 は非常に腐食性が高く、重傷を負う可能性があることはすでにわかっています。慎重に扱わないと私たちの肌。 BrF5 の結合角は 90° と計算され、この情報から分子の幾何学的形状も特定できました。これは、他の化合物や分子でも、それらの性質、電子配置、価電子殻電子がわかれば可能です。