無水物は、酸から水分子を除去することによって形成される 1 つの化学生成物です。では、無水物とは?酸素原子は、官能基を定義する 2 つのアシル基を接続します。無水物は「水なし」を意味します。別の化学物質から水が除去されたときに生成される化学物質として説明できます。無水物と水が結合して、塩基または酸を形成することがあります。混合無水物は、2 つの異なるカルボン酸から生成され、以下に示す一般構造で異なる R 基を有すると定義されます。酸無水物について学びましょう。
酸無水物の定義と意味
水と反応して酸性溶液を形成する非金属酸化物は、酸無水物と呼ばれます。これは、水中で酸性溶液を形成できる分子です。これは、酸素原子で結合された2つのアシル基からなる有機化学の官能基です。水と反応できる非金属は厳密に無水物と呼ばれますが、水と反応できない非金属は無水物とは見なされません。
有機化学によると、有機酸無水物は官能基R(CO)O(CO)R'を持っています。有機酸無水物は、脱水反応で2当量の有機酸から1当量の水が除去されるときに形成されることがよくあります.
一般的な酸無水物の構造
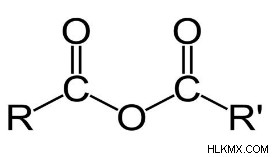
ここで、R と R‘ は任意のアルカン基です。
無水酢酸フォーミュラ
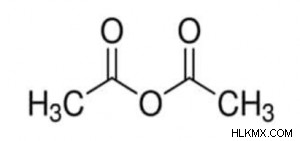
これは無水酢酸分子です。上記の R と R' をメタン (CH3) 基に置き換えると、無水酢酸の式が得られます。この分子は、酸無水物の基本的な例の 1 つです。
酸無水物の合成
酸無水物は、同じ酸素原子に結合した 2 つのアシル基 (R-C=O) を持つ物質です。カルボン酸が酸塩化物と結合すると、この反応はしばしば塩基の存在下で無水物をもたらします。 2つのカルボン酸を800℃以上の高温で加熱し、有機酸無水物を生成させます。このステップでは、水分子が反応から除去されます。カルボン酸は、P2 と反応して生成するために使用できます O5 .
脱水法は、酸無水物合成の化学反応を示しています。
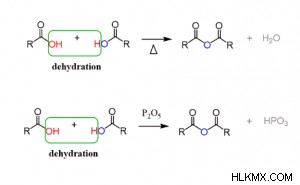
こちらR は任意のアルカン基です。
酸無水物の物性
代表的な物性として無水酢酸を考えてみましょう。
外観 – 無水酢酸としても知られる無水酢酸は、酢(酢酸)の特徴的な臭いを持つ無色の液体です。臭気は、無水酢酸が空気中の水蒸気や鼻の中の水分と結合して酢酸を再生成するときに生成されます。この水との反応については、別のページで詳しく説明しています。
水溶性 – 無水酢酸は水と結合して酢酸になるため、水に溶けるとは言えません。無水酢酸の水溶液は存在しません。
沸点 – 無水エタノールは 140 °C で沸騰します。それらは、双極子間分散力とファンデルワールス分散力を持つかなり大きな極性分子です。ただし、水素結合は形成しません。これは、同等のサイズのカルボン酸よりも沸点が低いことを示しています。たとえば、ペンタン酸はサイズが最も近い酸で、186 °C で沸騰します。
酸無水物の反応性
- 酸無水物と酸塩化物(酸塩化物)の比較。おそらく、あなたは最近塩化アシルの研究を完了し、同時に塩化アシルとして酸無水物に取り組んでいると思います。
- 酸無水物についてすべてをゼロから学ぼうとするよりも、何らかの修飾された酸クロリドと考える方がはるかに簡単です.それが、このセクション全体で私が取りたい態度です。
- 図の色分けを詳しく調べると、酸無水物と酸塩化物の構造を比較するのに役立ちます。
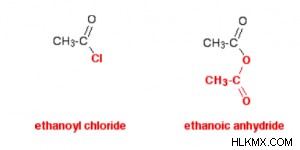
一番下の赤い基は、無水エタン酸反応で壊れることはありません。塩化アシルの塩素原子のように、多くの点で単一の原子のように見えます。塩化アシルは、塩素を別の物質に置き換えることによって反応することがよくあります。例として塩化エタノールを使用すると、最初の反応は次のようになります。

ガス状の塩化水素が生成され、後で組み合わせの他の成分と反応する可能性があります。無水物は反応を遅くしますが、主な違いは、塩化水素ではなく酢酸が副生成物として形成されることです。
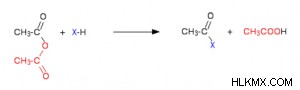
これは、塩化水素のように、他の環境要素と相互作用し続ける可能性があります.水、アルコールとフェノール、アンモニアとアミン、およびその他の物質は、塩化アシルと無水物の反応に関与します。これらの特定の状況のそれぞれにおいて、活性孤立電子対 (酸素または窒素) を持つ非常に電気陰性度の元素が存在します。
酸無水物の化学的性質
-OCOR基を変更することにより、酸無水物は求核置換反応を受けます。 -OCOR 基と比較して Cl 原子の電気陰性度が高いため、酸塩化物よりも反応性が低くなります。
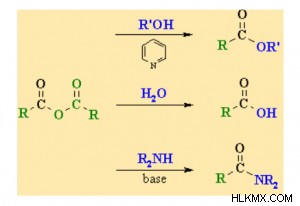
ここで R、R|、および R2 任意のアルカン基です。
炭酸の形成
二酸化炭素と水が反応すると炭酸が発生します。炭酸の化学式は以下の通りです。
CO 2 (g) + H 2 O→H 2 CO 3 (aq)
二酸化炭素は水と相互作用して水素を放出し、酸性炭酸または H2 を形成します。 CO3 .酸性雨はこのプロセスの結果です。小川、川、海のpHを変えるのに重要です。上記の式は、空気中の二酸化炭素の量を増やすと、生命を脅かす二酸化炭素が生成されることを示しています。私たちが現在取り組んでいる主な問題はこれです。
硫酸の生成:
三酸化硫黄と水が結合して硫酸を生成します。化学的に説明します。次に、三酸化硫黄ガスと水が相互作用すると、硫酸が形成されます。
そう 3 (g) + H 2 O→H 2 そう 4 (aq)
二酸化硫黄が空気中の酸素と結合すると、三酸化硫黄が形成されます。酸性雨は、雨が降ったときに水と反応して形成されます。これらは生態系に非常に悪い影響を与えます。
無水酢酸の詳細
- 無水酢酸は、酸無水物の最も単純な例の 1 つです。化学的に、無水酢酸とも呼ばれる無水酢酸の式は (CH3 CO)2 O. Ac2 と呼ばれることが多い O、最も簡単に分離できるカルボン酸の無水物です。これは、有機化合物の合成における一般的な試薬です。空気中の水分と反応して酢酸を生成する白い液体で、強い酢酸臭があります。
- 酢酸は 800 °C で脱水して無水酢酸を生成できます。あるいは、酸塩化物が酢酸ナトリウムなどの酢酸塩と反応すると、無水酢酸および塩が生成される。無水酢酸の式は、次のように表すこともできます:
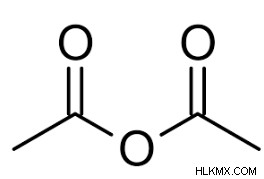
無水酢酸の性質
- IUPAC名:無水酢酸
- 分類:有機酸無水物
- 水溶性:水、ベンゼン
- 式:C4 H6 O3
- 無水酢酸の密度:1.08 g/cm³
- 無水酢酸 モル質量:102.09 g/mol
- 沸点:139.5 °C
無水酢酸の密度は 1.072 g/ml です。水は無水酢酸を吸収できません。無水酢酸の密度は水よりわずかに高く、密度は 0.999 g/mL です。ゼロ未満で適度に高い酸性度を持つ無水酢酸の pKa 値は -6.9 です。強酸では、ゼロ未満の pKa 値が見られます。酸はより強力で、pKa 値が低くなります。無水酢酸のモル質量は 102.09 g/mol であることがわかります。水のモル質量は約 18.015 g/mol です。したがって、無水酢酸のモル質量は水のほぼ 5 倍です。
無水酢酸の構造と性質
ほとんどの酸無水物と同様に、無水酢酸は非平面形状の可鍛性分子です。 2 つのカルボニル酸素間の双極子間の反発と比較して、中心の酸素を介して pi システムを結合すると、比較的控えめな共鳴安定性が得られます。理想的な平面のないコンフォメーション間で回転を結合するためのエネルギー障壁は比較的少ないです。
無水酢酸の用途
- 無水酢酸は、有機化学で示唆されているように、商業的に重要な製品につながるアセチル化に主に使用されます。
- 主な用途は、セルロースを酢酸セルロースに変換することです。セルロース アセテートは、たばこのフィルターの製造に使用され、写真フィルムやその他のコーティングされた材料のビルディング ブロックです。
- サリチル酸がアセチルサリチル酸とも呼ばれるアスピリンに変換されるのと同様に、このプロセスで使用されます。
- また、オートクレーブ含浸とその後のアセチル化による活性調整剤としても使用され、強くて耐久性のある木材を製造します。
- 無水酢酸は、違法な麻薬ヘロインとメタカロンの製造においてアセチル化剤として使用される主要な化学物質です。
有機酸無水物
- 有機化学物質である酸無水物は、有機酸無水物として知られています。同じ酸素原子に結合した2つのアシル基を持つ物質は、酸無水物と呼ばれます。式(RC(O)) 2 Oのカルボン酸無水物は、親酸がカルボン酸である典型的なタイプの有機酸無水物である。この形の対称無水物は、親カルボン酸の名前の酸という単語を無水という単語に置き換えることで示されます。したがって、(CH3CO)2O は無水酢酸とも呼ばれます。
- ギ酸無水物酢酸などの 2 つの異なるカルボン酸間の反応が存在する混合 (または非対称) 酸無水物が知られています。スルホン酸またはホスホン酸などの他の形態の有機酸も、無水物中の一方または両方のアシル基の供給源として機能することができます。リン酸などの無機酸は、無水物のアシル基の 1 つの供給源として機能します。
覚えておくべき重要なポイント
- 酸無水物は、有機化学で広く使用されています。
- 医薬品、工業用化学薬品、爆発物、香水など、多くの製品が彼らの助けを借りて作られています。
- エステルは、アルコールをアセチル化することによって作られます。
- アスピリン (アセチルサリチル酸) の合成。
- ヘロインは、モルヒネを脱アセチル化することによって作られます。