主な違い - ステレオジェニック センターとキラル センター
立体中心とキラル中心は、有機化学における立体異性を説明するために使用される 2 つの用語です。これらの 2 つの用語はしばしば同じと見なされますが、立体中心とキラル中心には違いがあります。すべてのキラル中心は立体中心ですが、すべての立体中心はキラル中心ではありません。立体異性体を生じさせるのはこれらの中心の存在であるため、立体中心とキラル中心の違いを知ることが重要です。
対象となる主な分野
1. ステレオジェニック センターとは
– 定義、特徴
2. キラル中心とは
– 定義、特徴
3. 立体中心とキラル中心
3.1. Stereogenic Center と Chiral Center の類似点
– 共通機能の概要
3.2. ステレオジェニック中心とキラル中心の違い
– 主な相違点の比較
重要な用語:キラリティー、キラル中心、異性体、ハイブリダイゼーション、立体異性、立体中心 
ステレオジェニック センターとは
ステレオジェン中心とは、結合した原子または基が交換されたときに異なる異性体を生成する任意の原子です。これらの異性体は、分子の構造は同じですが、それらの空間配置は互いに異なるため、立体異性体と呼ばれます。言い換えれば、立体異性体は、立体配置のみが互いに異なります。
立体中心である原子は、sp または sp ハイブリダイズすることができます。これは、二重結合または単結合のいずれかを持つ可能性があることを意味します。アキラル分子は、ステレオジェン中心を持つ場合もあります。したがって、すべてのキラル中心は立体中心です。しかし、立体中心は本質的にキラル中心ではありません。これの良い例は cis です –トランス ジオメトリ。
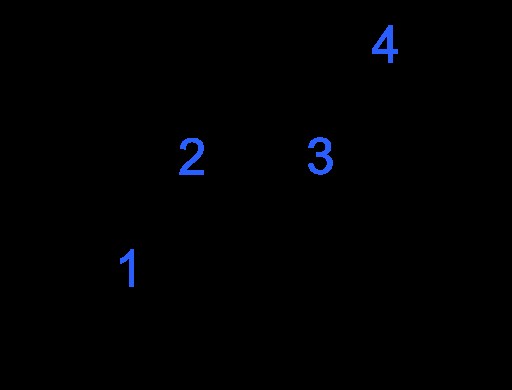
図 1:トランス-2-ブテン
上の画像は trans を示しています –2 -ブテン分子。キラル中心はありません。しかし、立体中心があります。炭素原子のうち、炭素原子に結合している 2 つの基が -H と -CH3 であるため、2 つと 3 つの炭素原子の両方がステレオジェン中心です。 これらの基は、この分子の立体異性体である新しい分子を得るために交換することができます。新しい分子は cis です –2 -ブテン。
キラル センターとは
キラル中心は、4 つの異なるグループに直接接続された炭素原子です。キラル中心を持つ分子は、その鏡像と重ね合わせることができません。このため、分子と鏡像は 2 つの異なる分子と見なされます。炭素原子は常に 4 つの基に結合できるように sphybridized になっています。
したがって、キラル中心を持つ分子は常に立体異性体を生成でき、キラル中心は常に立体中心です。 1 つの分子が複数のキラル中心を持つことができます。
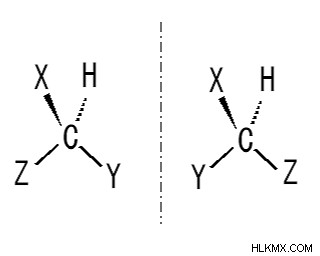
図 2:キラル中心を持つ分子
上の画像は、互いに異なる 3 つの他の基と共に水素原子 (H) に結合した炭素原子を示しています。 (X、Y、Z)。そこでは、炭素原子がキラル中心です。それは sp ハイブリダイズし、4 つの異なるグループに属しています。その鏡像は、分子と重ね合わせることができません。
ステレオジェニック センター vs キラル センター
Stereogenic Center と Chiral Center の類似点
- ステレオジェン中心またはキラル中心の存在により、立体異性体が生じます。
- キラル中心は常に不斉中心ですが、すべての不斉中心が不斉中心ではありません。
ステレオジェニック中心とキラル中心の違い
定義
ステレオジェニック センター: ステレオジェン中心は、それに結合している原子または基が交換されると、異なる異性体を生成する任意の原子です。
キラル センター: キラル中心は、4 つの異なるグループに直接接続された原子です。
ハイブリダイゼーション
ステレオジェニック センター: 炭素原子は、ステレオジェン中心で sp または sphybridized のいずれかです。
キラル センター: 炭素原子は常にキラル中心で sp 混成されます。
グループ数
ステレオジェニック センター: ステレオジェニック センターは、3 つまたは 4 つのグループに接続できます。
キラル センター: キラルセンターには常に 4 つのグループがあります。
債券
ステレオジェニック センター: 立体中心は、単結合または二重結合のいずれかを持つことができます。
キラル センター: キラル中心には単結合しかありません。
キラリティー
ステレオジェニック センター: 立体中心は、キラル分子またはアキラル分子のいずれかに見られます。
キラル センター: キラル中心はキラル分子にのみ見られます。
グループの交換
ステレオジェニック センター: 立体中心を持つ一部の分子は、結合基が交換されると立体異性体を生成します。 (例:cis-trans 異性体)
キラル センター: 結合基が交換されても、キラル中心を持つ分子は違いを示しません。
結論
すべてのキラル中心は立体中心ですが、すべての立体中心はキラル中心ではありません。立体中心とキラル中心の違いを識別するために使用できる多くの明確な特徴があります。