コア コンセプト
この記事では、「互変異性化」の意味、エノール安定性の傾向、酸性および塩基性条件下での重要なメカニズムなど、ケト エノール互変異性化について学びます。
ケトエノール互変異性化とは?
ケトエノール互変異性化は、ケトン分子とエノール分子の構造を変換する反応です。このような反応のメカニズムを説明する前に、まず「互変異性化」の意味を明確にしましょう。
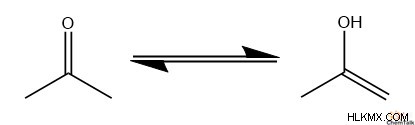
化学者は「互変異性化」という用語を使用して、動的平衡状態で相互変換する 2 つの分子構造のプロセスを説明します。多くの場合、これには分子上の 2 つのサイト間での化学基の移動が含まれます。
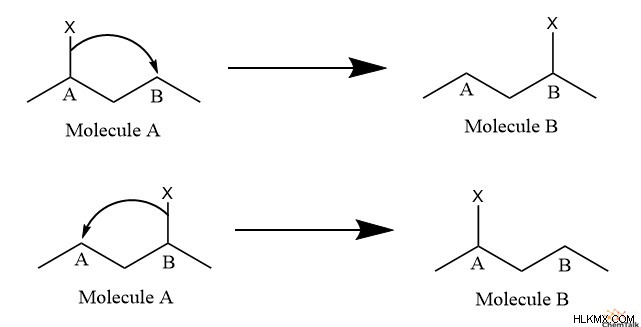
別の言い方をすると、いくつかの官能基 X を持つ分子 A があるとします。分子 A では、基 X がサイト A に結合します。しかし、基 X が結合するのに適した別の場所が存在し、サイト B と呼ばれます。サイト A をサイト B に変換すると、分子 A がその互変異性体である分子 B に変化します。部位 B に到達すると、基 X も部位 A に戻ることができます。分子構造を変換する部位間の基 X の移動は、互変異性化と呼ばれます。
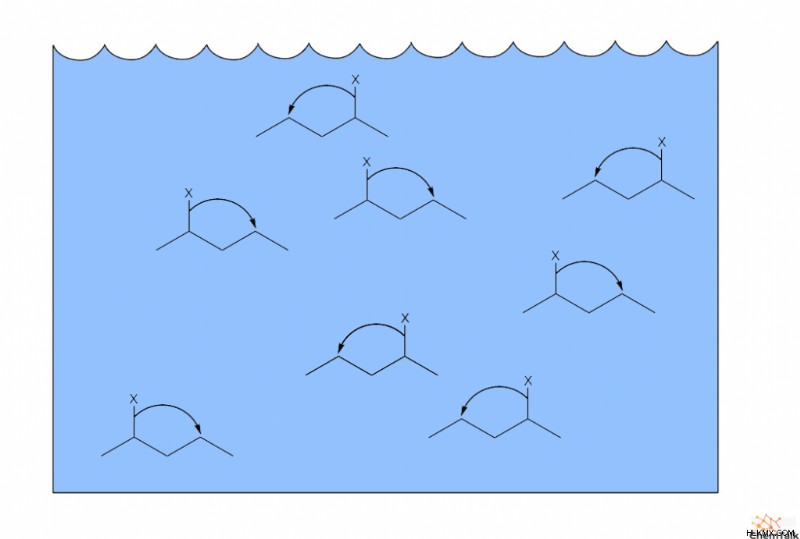
溶媒に溶解した分子など、分子 A がたくさんある場合、分子 B に変換され、再び分子 B に戻ります。ただし、分子 A と分子 B の相対的な割合は一貫したままです。これは、最終的に変換率が相殺されるためです。これが、化学者が言う「動的平衡」です。
多くの場合、分子 A は分子 B よりも安定性が高く、平衡状態で分子 A が B よりも多いことを意味します。この不均等な平衡状態は、ケトンとエノールの間を含む互変異性体のペアで一般的に発生します。ただし、ケト エノール互変異性化では、異なる構造要因によって、どの分子が他の分子より数が多いかが決まります。
ケトエノール互変異性体構造
一般に、最も一般的な分子構造の多くでは、エノールよりもケトンが非常に好まれます。ただし、α-炭素 (カルボニルから一度取り除かれた炭素) の構造によって、ケトンの好感度が変わる可能性があります。
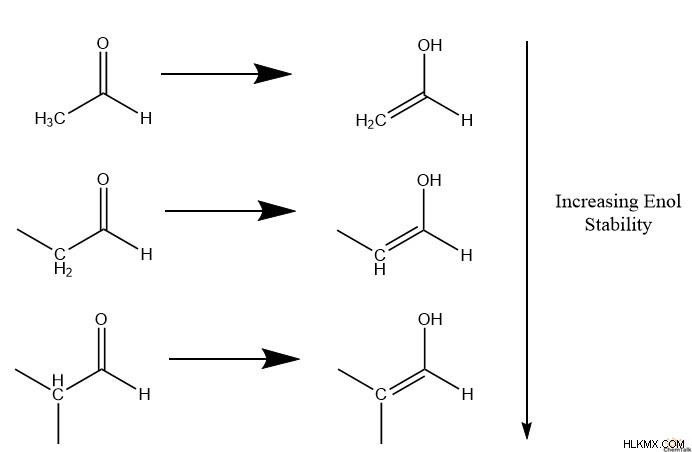
そのような構造的傾向の 1 つは、より多くの非水素を含む ɑ-炭素がエノールとしてより安定していることです。たとえば、α-炭素が 3 つの水素を持つメチル構造を持っている場合、エノールを形成する安定性は、2 つの水素を持つメチレン α-炭素よりも低くなります。メチレン ɑ-炭素によって形成されたエノールは、1 つの水素と 2 つの炭化水素結合を持つメチン ɑ-炭素より少ないエノールを安定化します。
しかし、エノール型がケトン型より優勢な分子がいくつか存在します。そのような例の 1 つは、特定のアルドール縮合から頻繁に形成される 1,3-ジカルボニル分子です。これらの分子では、エノールが形成され、水素が酸化物イオンにシャッフルされます。この新しい水酸化物構造は、水素結合を提供する隣接するカルボニルから安定化します。最終的に、このエノール-ケトンの組み合わせは、6 員環の特徴を持つこの自己安定構造を形成します。

芳香族エノールも安定性を持つ傾向があります。芳香族性がケトンの安定性を上回るほどの安定性を提供するからです。具体的には、結果として得られるアルケンが芳香族電子サイクルを完了する場合、エノールが優先されます。これは、フェノールが安定した構造を形成する傾向があるのに対し、2,4-シクロジエノンはまれなままである傾向がある理由を説明しています.
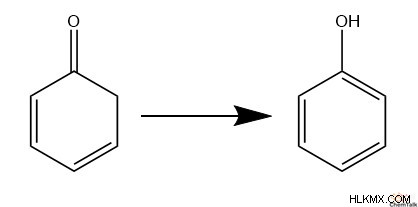
ケトエノール互変異性化メカニズム
酸性条件下での互変異性
酸性条件下でのケト - エノール互変異性は、ケトンとエノール間の変換を促進するプロトン化を本質的に持っています。
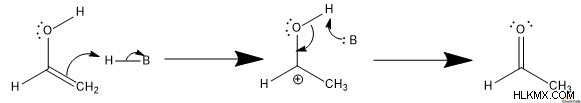
エノールを形成するために、酸はカルボニル上の孤立電子対をプロトン化します。次に、酸の共役塩基がα-炭素を脱プロトン化します。これにより電子の移動が促進され、最終的にエノールが形成されます。

ケトンを形成するために、酸はアルケンをプロトン化し、α-炭素とプロトンの間に C-H 結合を形成します。次に、共役塩基が水酸化物を脱プロトン化します。次に、酸化物アニオンの孤立電子対がカルボカチオンとパイ結合を形成し、結果としてケトンになります。
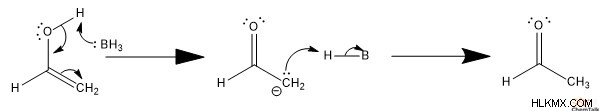
基本条件下での互変異性化
基本的な条件下でのケト - エノール互変異性は、本質的に de を持っています -ケトンとエノール間の変換を促進するプロトン化。
エノールを形成するために、一般的な Brønsted-Lowry 塩基が ɑ-炭素を脱プロトン化します。これにより、カルボニルのπ電子が駆動され、脱プロトン化された炭素とアルケンπ結合が形成されます。次に、共役酸が酸化物アニオンをプロトン化し、エノールを形成します。
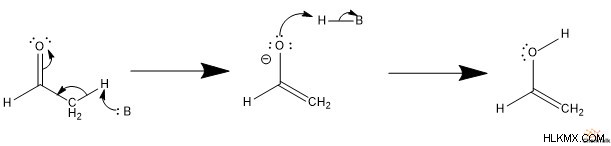
ケトンを形成するために、塩基は水酸化物を脱プロトン化し、孤立電子対を解放します。次に、これらの電子はカルボニルを形成し、孤立電子対をα-炭素に押し付けます。次に、共役酸が ɑ-炭素をプロトン化し、ケトンを形成します