1モルのイオンが水和するときに生じるエネルギー量が水和エネルギーまたは水和エンタルピーです。水分補給は一種の溶媒和です。水和エネルギーは、溶媒が水であるエネルギーの溶解の形です。構造予測の最も困難な要素の 1 つは、水和エネルギーの数を決定することです。塩が水に溶けると、陰イオンと陽イオンが水の正と負の双極子と反応します。水和エネルギーは、これらの相互作用と結晶性固体内の相互作用との間のトレードオフの結果です。 Wendell Latimer は、水和エネルギーが陰イオンと陽イオンのイオン半径に関連していることを発見しました。
水和エンタルピーとは?
水和エンタルピーは、1 モルの気体イオンが H2O (水) と混合されて水和イオンを生成するときに生成される電力/熱/エネルギーの量として定義されます。
リチウムの例を見てみましょう。これは、高い還元力を示す、より負の電力値 E– を持つアルカリ金属です。
還元力は、昇華エネルギー、水和エネルギー、イオン化エネルギーの 3 つのエネルギーの合計として表されます。
それらを以下に示します:
まず、昇華エネルギーについて
M(s) → M(g)
第二に、イオン化エネルギー
M(g) → M+(g)
3 番目のステップ、水和エンタルピー
M+(g) + H2O → M+(aq)
EO =IE+ ΔHn +ΔHs
どこで EO =還元力
IE =イオン化エネルギー
ΔHn =水和エネルギー
ΔHs =昇華エネルギー
リチウムはサイズが小さいため、イオン化エンタルピーが高くなります。ただし、サイズが小さいため、水和量が多く、水和エンタルピーが高くなります。水和の高いエンタルピーは、(第 2 段階で) 電子を除去するために必要なかなりのエネルギーを説明します。したがって、リチウムは他のアルカリ金属よりも溶液中で電子を失う傾向が大きくなります。その結果、リチウムは最も強力な還元剤です。
したがって、リチウムの高い還元力はその高い水和エネルギーに関連しており、リチウムの大きな水和エネルギーはサイズが小さいことに比例します。
水和エンタルピーの大きさに影響する要因
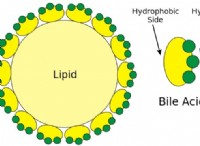
水和エンタルピーは、負または正のイオンと水分子が引力を形成するときに生成されるエネルギーです。これらの引力は、酸素原子、陽イオン、および水分子間の厳密な座標共有結合であるか、単にイオン双極子引力を失う可能性があります。イオン双極子引力は、水分子内の負イオンと正水素イオンの間に形成されます。
通常、イオンと水分子の間の引力の程度は、水和エンタルピーの大きさに依存します。
小さいイオンの場合、引力は一般に高い。たとえば、水和エンタルピーは、周期表を下に進むにつれて減少します。リチウム イオンは、周期表の第 1 族で最も高い水和エンタルピーを持ちますが、より小さいフッ化物イオンは、第 7 族で最大の水和エンタルピーを持ちます。イオン サイズが大きくなるにつれて、水和エンタルピーは両方のグループで減少します。
イオンの電荷は、イオン間の引力に正比例します。つまり、引力は電荷の増加とともに強くなります。たとえば、グループ 2 のイオン (Mg2+ など) は、グループ 1 のイオン (Na+ など) よりも実質的に大きな水和エンタルピーを持っています。
水和エンタルピーの適用
水和エンタルピーの例は、水とセメントの反応です。このプロセスは発熱性であるため、大量の熱が放出されます。巨大なコンクリート ブロックを構築するために大量のセメントが使用されるダムやその他の構造物などの大量建造物では、放出される熱が重要になります。
硬化過程で熱が発生します。レンガの外側の端は内側の端よりも早く冷えるため、レンガに温度勾配が生じ、ひび割れや構造的な破損につながる可能性があります。この課題を回避するために、低熱タイプのセメント、フライアッシュやスラグなどのポゾラン混合物を含むセメント、および水ではなく氷で準備されたコンクリートが、巨大な建造物に好まれます.
結論
上記のトピックでは、水和エンタルピーについて説明しました。これは、化学方程式で広く使用されている化学の最も重要な概念の 1 つです。水和エンタルピーは、1 モルのガス状イオンが水と混合されて水和イオンを生成するときに生成されるエネルギー量として定義されます。水和エンタルピーを決定するさまざまな要因は、水和エンタルピー、イオン半径、およびイオン荷電です。水とセメントの存在下で熱を発生させる化学反応は、水和エンタルピーの原理に基づいています。