リガンドの種類
配位化合物は、配位子に共有結合している金属イオンで構成されています。配位子は、遷移金属と配位結合を形成できる荷電または中性の分子またはイオンです。 「リガンド」という言葉は、「結合する」を意味するラテン語の Ligandus に由来します。それらは、中心金属の空の混成軌道に電子対を供与します。
リガンドには様々な種類があります。それらは、歯密度、複雑な分子構造、化学的性質、電界強度に基づいて分類できます。
デンティシティ
デンティシティは、金属との結合プロセスに関与するドナー グループの数として定義されます。リガンドは、そのデンティシティに基づいて次のように分類できます:
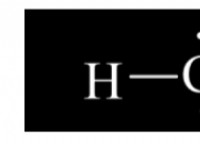
- 単座リガンド :配位子がドナー部位/グループを 1 つしか持たない場合、単座と呼ばれます。金属の 1 か所だけを攻撃する (または噛む) ため、「片歯」とも呼ばれます。単座配位子の例には、Cl-、NH3 などがあります。これらは、孤立電子対を金属に供与します。
- 多座リガンド :配位子が複数のドナー部位/グループを持っている場合、それは多座と呼ばれます。さらに、ドナー サイトの数に基づいて、次のタイプに分類できます。
多座リガンド :配位子が複数のデンティシティを示すことができる場合、それは多座と呼ばれます。 EDTA (エチレンジアミン四酢酸) は、1 ~ 6 の範囲のさまざまな数の電子対を供与できる例です。 2 つの窒素または 4 つのアセテート基の酸素を介して金属中心と結合できます。実際の歯密度は、pH などの外的要因によって異なります。

- アンビデント リガンド: 複数のドナー部位を持つが、一度に結合に関与できるのはそのうちの 1 つだけであるリガンド。たとえば、SCN- は、硫黄中心と窒素中心の両方から供与できるため、両座配位子です。 NO2- は、酸素中心と窒素中心の両方から供与できるため、両座です。
リガンドにおけるキレート効果
多座配位子は、複数のドナー部位を介して同時に中心金属と結合できるため、キレート効果を示します。中央の金属イオンは、金属の周りにリング状の構造が形成されるため、キレート効果を示す配位子に対してより大きな親和性を示し、より優れた構造安定性を提供します。
キレート配位子の例には、EDTA およびジエチレントリアミンが含まれます。
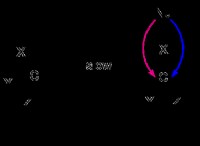
架橋リガンド
リガンドは、2 つの金属イオン間のブリッジとして機能します。カルボニルと水素化物は、いくつかの化合物で架橋配位子として機能します。
Fe2(CO)9 のカルボニル架橋では、9 つのカルボニル配位子のうち、そのうちの 3 つが架橋として機能します。


電荷に基づく配位子の種類
電荷に基づいて、以下にリガンドのいくつかのタイプを示します:
<オール>リガンドの分光化学シリーズ
配位子は、金属の d 軌道を分割する能力に基づいて、分光化学系列に配置できます。 d 軌道をより大きなエネルギー差を持つ 2 種類の軌道に分割する配位子は、Strong Field Ligand と呼ばれます。 d軌道をエネルギー差の小さい2種類の軌道に分割する配位子を弱電界配位子と呼びます。
I-
強い電場配位子は、電子を d 軌道でペアリングさせ、低スピンで反磁性の複合体を与えることができます。
配位子に関して言えば、デンティシティは重要な概念です。いくつかのタイプの配位子の例が、さまざまなデンティシティーに対応しています。多座配位子は、錯体を大幅に安定化するのに役立つキレート効果を示すことができます。リガンドは、2 つの金属イオン間のブリッジとしても機能します。
リガンドは、電荷に基づいて分類することもできます。重要な分類は、複雑な分子のハイブリッド化と形状を最終的に決定する電界強度に関するものです。結論