滴定は、既知の濃度の溶液を使用して、未知の溶液の濃度を決定する技術です。終点に達するまで、既知の溶液 (滴定液) を検体 (未知の溶液) に滴加します。
好きな飲み物はレモネードですか?それとも、減量のために時々食事に加えますか?理由が何であれ、レモネードの形で摂取しているレモン果汁の濃度を知っていますか?濃度が限界を超えると、自分の胃にダメージを与える心配はありませんか?
まずは…リラックス!レモネードのレモン果汁の濃度を気にする必要はありません。
ただし、特定の薬品、食品防腐剤、水槽の pH レベル、およびさまざまな工業的手順に関しては、溶液中のさまざまな成分の濃度が大きな役割を果たします。
ここで滴定の出番です!滴定は、特定の厳密な手順に従って溶液の濃度を決定します。この記事では、滴定の原理と方法論について説明します。

滴定の様子 (写真提供:Torychemical/Shutterstock)
滴定の原理とは?
滴定は、既知の濃度の溶液を 1 滴ずつ加えることによって、未知の溶液の濃度を決定する定量分析です。このプロセスにより、既知の濃度の酸または塩基は、未知の濃度の酸または塩基を完全に中和します。中和中に起こる実際の反応は、酸からの水素イオンと塩基からの水酸化物イオンが結合して水を形成することです。プロセス全体で均一な pH を維持することが重要です。したがって、検体と滴定液は同じ濃度でなければなりません。強力な滴定と希釈された検体、またはその逆を含むと、検体の物理的性質に影響を与えます。このプロセスは通常、pH 電極または指示薬によって監視されます。
既知の濃度の溶液は滴定液であり、濃度が決定される溶液は検体です。このプロセスの当量点は、滴定液が検体中の塩基または酸を完全に中和したときに得られます。
滴定はどのように行われますか?
検体を測定し、ビーカーに充填します。メチル オレンジやフェノールフタレインなどの酸塩基指示薬を数滴分析対象物に加えます。
フェノールフタレインは酸では無色のままですが、塩基が存在するとピンク色になります。同様に、メチル オレンジは赤みがかったオレンジ色の粉末で、酸では濃い赤色になり、塩基では淡い黄色になります.
標準溶液をビュレットに取り、プロセスを開始します。標準溶液は、検体の入ったビーカーにゆっくりと滴り落ちます。このプロセスは、検体の色が変化して終点に到達したことを示すまで実行されます。これは、検体中のすべての塩基または酸が滴定液によって完全に中和されたことを意味します。
終点での標準液の体積変化を記録します。この容量は、検体を中和するために使用された滴定液の量を示します。これらの値は、その後の計算で使用されます。
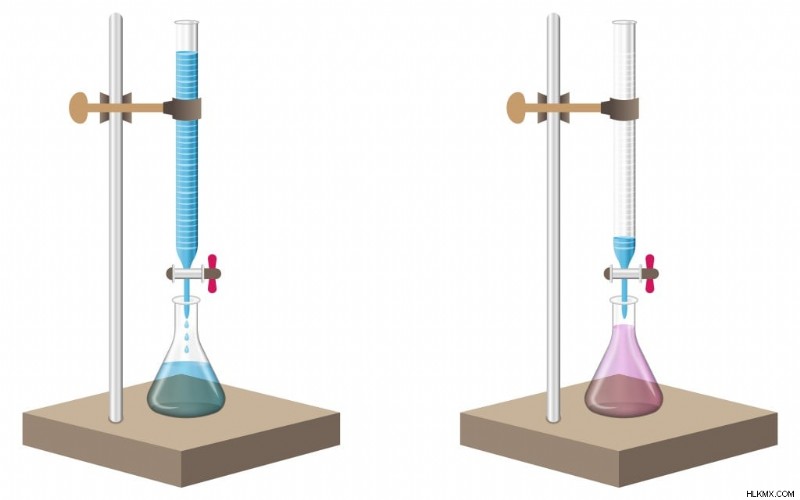
滴定液の添加後の検体の色の変化 (写真提供:MeKa Design/Shutterstock)
滴定式:分析物の濃度はどのように計算されますか?
他のすべての定量分析と同様に、滴定には未知の濃度を決定するための標準式があります。一般的に使用される式は次のとおりです:
滴定液の体積 * 滴定液のモル濃度 =検体の体積 * 検体のモル濃度

1.25 M 水酸化ナトリウム 45.6 ml を使用して 20 ml の塩酸を中和したとします。 HCl の濃度は、
45.6 X 1.25 =20.0 * 検体のモル濃度。
上記の方程式を解くと、検体の濃度が得られます。
滴定の種類
関連する反応のタイプに基づいて、滴定イオンは 4 つの異なるタイプに分類されます。
- 酸塩基滴定: これは、酸または塩基と分析対象物との間の中和に基づいています。
- 錯滴定: これは、反応に関与する金属イオンの数を決定するために広く使用されています。 EDTAは指標として使用されます。この滴定の終わりに、当量点を示す非解離複合体が形成されます。例:
Ag+ + 2CN– → [Ag(CN)2]–
- レドックス滴定: このタイプでは、電子の移動は溶液の反応イオンで行われます。使用する試薬の種類によってさらに 3 種類に分類されます。
過マンガン酸塩:MnO4–+ 8H + 5e → Mn2++ 4H2
二クロム酸塩:K2Cr2O7+ 4H2SO4 → K2Cr2(SO4) + 4H2O + 3[O]
ヨーディメトリックとヨードメトリック:l2 + 2e → 2l–
- 沈殿滴定: この反応は、反応する 2 つの物質が接触すると、不溶性の沈殿物を形成します。
AgNO3 + NaCl → AgCl + NaNO3
滴定ユーティリティ:実用的なアプリケーションと例
滴定は、おそらく私たちの日常活動に何らかの形で適用されます。血液検査や尿検査などのさまざまな臨床検査では、滴定を使用して目的の化学物質の濃度を決定します。また、食品業界で食品中の特定の化学物質の量を決定するためにも使用されます。
多くの場合、炭水化物、脂肪、ビタミンの含有量を測定するために使用されます。滴定は、医療分野でも広く適用されています。妊娠検査、血糖値検査、その他の尿検査アプリケーションでは、滴定が使用されます。また、高校生の実践適性を分析するための学問の一部としても含まれています。
アンモニア濃度、硝酸塩濃度、pH レベルなどの海水特性が計算され、それに応じて環境が変更され、最適な条件が維持されます。
一般にモル濃度 (溶液中の 1 リットルあたりの溶質のモル数) で表される濃度は、反応速度と平衡状態を決定するため、化学において非常に重要です。滴定は、未知の濃度を決定するための最も有名で広く使用されている方法です。